Электронное распределение
Cтраница 1
Электронные распределения в этих молекулах не вполне соответствуют ароматическому типу, но скорее включают отдельные аллильные области, начинающиеся и кончающиеся на атомах фосфора или серы. [1]
Электронное распределение, характеризуемое волновой функцией г г, имеет в направлении оси Z форму объ-восьмерки, а перпендикулярно ей - форму тора. [2]
Данное электронное распределение, вероятно, применимо к любым секстетам, включая бензол. Различие состоит лишь в том, что в бензоле двойная связь может свободно передвигаться, в нафталине подвижность ее частично ограничена, а в фенантрене она фиксирована в среднем кольце. [3]
Характер электронного распределения в молекуле может меняться в зависимости от того, в каком из электронных и колебат. [4]
Для изображения электронного распределения в невозмущенной или нереагирующей молекуле рекомендуется применять иной способ-обозначения или иные знаки, чем для молекулы в момент реакции. [5]
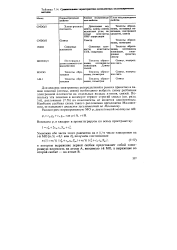 |
Сравнительная характеристика всевалеитиых иолуэмишрических методов. [6] |
Для анализа электронных распределений в рамках принятых в химии понятий ( атомы, связи) необходимо выбрать схему разбиения электронной плотности на отдельные вклады атомов, связей. Поскольку эти понятия в молекуле теряют строгий смысл ( см. разд. Наиболее удобная схема такого разложения предложена Маллике-ном, ее называют анализом заселенностей по Малликену. [7]
Наглядное изображение электронного распределения в кова-лентной молекуле Н2, полученное с помощью ЭВМ в рамках теории молекулярных орби-талей по методу ЛКАО. [8]
Другим показателем среднего электронного распределения является величина химического сдвига в спектрах ядерного магнитного резонанса. Так, например, сдвиг линий протонного и фторного резонанса в область более сильного поля обусловлен повышенной электронной плотностью около ядер. По его мнению, заметно больший элек-тронодонорный характер дейтерия обусловлен меньшим атомным объемом дейтерия в ковалентных соединениях. Однако Гутовский [39] объясняет эти сдвиги меньшей среднеквадратичной амплитудой колебания для дейтерированных молекул. Результаты расчета, выполненного им для одного частного случая, хорошо согласуются с экспериментом. Модель, использованная Гутовским при расчете, аналогична учету второго члена в уравнении ( П-4) для разности дипольных моментов изотопной пары гармонических осцилляторов. Маршалл [40] теоретически рассчитал для Н2, HD и D2 влияние изотопного замещения на константу ядерного экранирования ( ст), ответственную за появление химических сдвигов. [9]
В случае неискаженного сферического электронного распределения, которое существует, например, в атоме водорода, индуцированное движение заряда приводит к чисто диамагнитному эффекту. [10]
Резонансный гибрид - атомное и электронное распределение, соответствующее реальной молекуле. Резонансные структуры характеризуются одинаковым расположением атомов, что соответствует расположению атомов в реальной молекуле, но различным распределением электронов по сравнению с резонансным гибридом. Примером может служить бензол. [11]
В силу такого электронного распределения гетеро-атом обладает долей положительного заряда, а концевому этиленовому атому углерода присуща доля отрицательного заряда. [12]
Вследствие понижения симметрии электронного распределения увеличивается парамагнитный вклад в экранирование, и наблюдаются сдвиги в слабое поле. Ядра 19F во фторированных карбокатионах сильно дезэкранированы. [13]
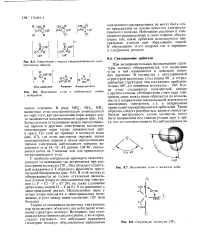 |
Структуры с тремя стереоактивными электронными парами.| Валентные углы в соединениях азота с водородом.| Валентные углы в молекуле воды.| Структура молекулы C1F3. [14] |
Небольшие различия в электронном распределении в свою очередь обусловлены тем, какие орбитали используются центральным атомом при образовании связей. [15]
Страницы: 1 2 3 4