Электронное распределение
Cтраница 3
Они приводят к сходному результирующему электронному распределению для данной молекулы. [31]
Следует заметить, однако, что электронное распределение в атомных состояниях НеН имеет s - характер, в то время как в связях XeF2 и XeF4 участвуют главным образом р-электроны. Так как р-электроны создают более благоприятные условия для связывания, возможно, что в XeF2 и XeF4 радиальная корреляция будет играть более важную роль. [32]
Поэтому в однодетерминантном приближении все детали электронного распределения определяются только этими двумя функциями. [33]
Такое соотнесение естественно, поскольку топология электронных распределений существенно меняется лишь при таких изменениях ядерной конфигурации, к-рые можно связать с изменением системы связей. [34]
Аналогично можно определить вероятности для двух других электронных распределений: 1) два электрона в объеме УА, 2) два электрона в объеме УВ. [35]
Ясно, что для получения картины точного электронного распределения в молекуле илида необходимо знание длин связей, углов между ними и электронной плотности илидной связи. Проблема получения таких данных усложняется тем, что в молекуле илида, достаточно устойчивого для рентгенографического исследования, у илидного атома углерода должны находиться весьма большие группы. [36]
Нитро-группы в ДФПГ не только влияют на электронное распределение в радикале, но - и оказывают стерическое действие. [37]
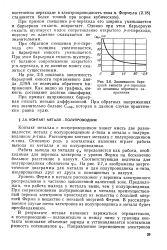 |
Зависимость барьерной емкости / 7-п-перехода от величины обратного напряжения. [38] |
Уровень Ферми в металле расположен у вершины электронного распределения в частично заполненной валентной зоне. Предположим, что работа выхода у металла выше, чем у полупроводника. При соприкосновении полупроводника и металла преимущественный переход электронов происходит из вещества с большей энергией Ферми в вещество с меньшей энергией Ферми. [39]
 |
Туннельный пробой р-п-перехода. [40] |
Уровень Ферми в металле расположен у вершины электронного распределения. Предположим, что работа выхода из металла выше, чем из полупроводника. При соприкосновении полупроводника и металла преимущественный переход электронов происходит из вещества с большей энергией уровня Ферми в вещество с меньшей энергией уровня Ферми. [41]
Однако такая запись вовсе не предполагает, что электронное распределение в молекуле SO2 быстро смещается из стороны в сторону, так что при этом попеременно то на одной, то на другой связи возникает повышенная электронная плотность. Она лишь означает, что электронное распределение симметрично по отношению к обеим связям и не может быть правильно охарактеризовано какой-либо одной из двух электронных формул. Подобные записи часто используются при описании резонансных систем. [42]
Это позволяет надеяться на обнаружение очень небольших изменений электронного распределения в молекулах при образовании комплекса. Однако, к сожалению, в наблюдаемые значения ККВ помимо валентных электронов на резонансном атоме вносят вклад и другие факторы, и поэтому ее изменения при комплексообразовании и роль этих факторов трудно предсказуемы. К последним относятся: 1) вклад остальных электронов молекулы, которые также испытывают влияние комплексообра-зования; 2) влияние соседних молекул; 3) влияние молекулярного движения, которое усредняет ККВ резонансного ядра. Все эти эффекты ограничивают точность оценки влияния комплексообразования на распределение валентных электронов. Столь сильные ограничения на применение спектроскопии ЯКР к изучению электронного распределения должны учитываться при обсуждении экспериментальных результатов. Вместе с тем спектроскопия ЯМР имеет еще другие возможности, связанные с влиянием температуры, давления и магнитного поля на ККВ, а также с влиянием температуры на время релаксации, и они с успехом используются при определенных обстоятельствах для изучения молекулярных комплексов. Со времени первого наблюдения ЯКР в комплексах [50] были проведены многие исследования и получены интересные результаты, достойные того, чтобы их проанализировать здесь. [43]
 |
Два типа электронного перехода в SOJ. [44] |
Дипольный момент молекулы может изменяться в зависимости от электронного распределения. В отличие от этого переход Is - - ls симметричен, при нем не возникает преходящего дипольного момента, и он запрещен. В молекулах нужно искать такой же преходящий дипольный момент ( он называется дипольным моментом перехода), связанный с перераспределением заряда. Пример дан па рис. 17.4: один из приведенных переходов для молекулы S0 разрешен ( он имеет дипольный момент, качественно аналогичный foweгIгy для перехода 5 - - pz в атоме), однако второй ( гга-поминающий переход s - s в атоме) имеет нулевой диполь и поэтому запрещен. [45]
Страницы: 1 2 3 4