Неравномерное распределение - электронная плотность
Cтраница 1
Неравномерное распределение электронной плотности в ковалентной связи создает диполь связи, в качестве единицы измерения4 которого служит произведение заряда на расстояние ( для более детального обсуждения ем. [1]
Неравномерное распределение электронной плотности между концевыми С ] и С3 атомами углерода в я-кротильных комплексах сказывается на характере их взаимодействия с реагентами. [2]
 |
Полярная молекула с постоянным электрическим моментом диполя. [3] |
Односторонняя поляризация приводит к неравномерному распределению электронной плотности в молекуле. [4]
В соединениях ароматического ряда наблюдается аналогичное неравномерное распределение электронной плотности: при наличии хлора все ядро благодаря большему - / - эффекту хлора заряжено положительно, но в орто - и пара-положениях ( в положении 2 и 4 бензольного ядра) положительный заряд оказывается частично погашенным, благодаря сопряжению атома хлора с бензольным ядром. [5]
Наличие двух гетероатомов приводит к очень неравномерному распределению электронной плотности. Наряду с центром со значительной я-избыточностью имеется атом с высокой я-дефицитностью. Не-поделенная пара электронов пиррольного гетероатома азота значительно больше вовлечена в образование л-секстета, чем у пиррола. Здесь сказывается влияние пиридинового гетероатома азота. Имидазол, а также другие гетероциклы, содержащие гетероатомы пиррольного и пиридинового типов в одном ядре ( оксазол, тиазол, пиразол и др.), называют к-амфотерными гвтероциклами. Наличие двух гетероатомов азота определяет амфотерные свойства имидазола: пир-рольный азот обусловливает кислотные свойства, о чем свидетельствует способность имидазола к образованию солей с щелочными и щелочноземельными металлами. [6]
 |
Полярная молекула. [7] |
Односторонняя поляризация молекулярного электронного облака приводит к неравномерному распределению электронной плотности в молекуле. [8]
Еще большее значение гипсохромное смещение максимума поглощения, в результате неравномерного распределения электронной плотности, приобретает во внутриионоидных красителях - азометинах и мероциа-нинах. [9]
 |
Константы этилена и его гомологов. [10] |
Измерение дипольных моментов ( i) несимметрично метилированных этиленов дает прямое указание на неравномерное распределение электронной плотности в их молекуле. [11]
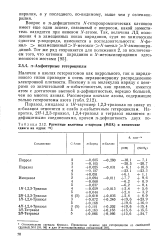 |
Расчетные величины я-зарядов ( МОХ и химические сдвиги на ядрах 13С. [12] |
Наличие в азолах гетероатомов как пиррольного, так и пиридинового типов приводит к очень неравномерному распределению электронной плотности. Поэтому в их молекулах наряду с центрами со значительной л-избыточностью, как правило, имеется атом с достаточно высокой л-дефицитностью, нередко большей, чем во многих азинах. [13]
Наличие катионов в полостях цеолитов, являющихся адсорбционными центрами для адсорбции молекул с неравномерным распределением электронной плотности, представляет наиболее характерную особенность цеолитов как микропористых адсорбентов. Обязанные этим центрам более сильные по сравнению с дисперсионными адсорбционные взаимодействия приводят к более крутым, чем для активных углей, изотермам адсорбции в начальных областях равновесных давлений. Na составляет 2.4 ммоль / г и нелокализованных 2.3 ммоль / г из расчета на полностью дегидратированный цеолит. [14]
Атом водорода у ненасыщенного атома в молекуле алкинов ( СНСН; R - ССН) вследствие неравномерного распределения электронной плотности н - с С - н0 приобретает способность отрываться в присутствии сильных оснований в виде протона. [15]
Страницы: 1 2 3