Рассмотрение - кинетика
Cтраница 1
Рассмотрение кинетики и равновесия реакций присоединения азотных оснований типа гидроксиламина и семикарбазида осложняется двух-стадийным характером этих процессов, а также тем, что механизм катализа различен для разных реакций. Влияние заместителей на каждую отдельную стадию образования семикарбазона из замещенных бензальдегидов подробно изучено [3, 53, 191] и вкратце рассматривалось выше. [1]
Рассмотрение кинетики синтеза и разложения аммиака, как видно, показывает, что теория процессов на неоднородных поверхностях в состоянии объяснить совокупность наблюдаемых на опыте кинетических закономерностей. [2]
Рассмотрение кинетики набухания в указанных аспектах приводит к проблеме решения уравнения нестационарной диффузии в условиях перемещающихся границ. Этот метод основан на разложении искомого решения в ряд по некоторым системам мгновенных собственных функций соответствующей задачи. [3]
Рассмотрение кинетики флокуляции основано на известных представлениях, развитых Смолуховским для описания кинетики коагуляции дисперсных систем и впоследствии Фуксом, учитывавшим взаимодействие между коагулирующими частицами. [4]
Рассмотрение кинетики извлечения вольфрама в раствор свидетельствует о том, что в ускорении процесса извлечения вещества из пористых частиц существенную роль играют мелкомасштабные пульсации среды, величина которых соизмерима с поперечным сечением пор. При этом относительное тангенциальное колебательное смещение частиц среды трансформируется в однонаправленное движение раствора, заменяя тем самым молекулярный перенос диффундирующих частиц вещества значительно более ускоренным конвективным переносом при наложении акустического поля. [5]
Рассмотрение кинетики гетерогенных реакций невозможно вне связи ее с проблемами термодинамики и адсорбции. [6]
Рассмотрение кинетики каталитического риформинга затрудняется тем, что параллельно протекают разнородные реакции, и глубина превращения характеризуется степенью не только ароматизации, но и гидрокрекинга. Например, энергия активации дегидрирования циклогексана составляет 75 7 кДж / моль и температурный градиент скорости этой реакции равен - 41 С. [7]
Рассмотрение кинетики химических реакций для нестационарных условий без учета принципа стационарности представляет определенный интерес. Известно что катализ - это химическое явление, что в полной мере относится к катализаторам Фриделя-Крафтса - Густавсона - А12С16, H2SO4, НС1, HF, BF3 и другим и к их смесям, способным образовывать неустойчивые промежуточные соединения с молекулами реагирующих веществ. [8]
Рассмотрение кинетики однотипных реакций в ПИМ и ПРМ на основе индексов реакционной способности приводит к уравнениям (4.23), (4.26) или (4.39), которые получены на основе модели механизма реакции. [9]
Рассмотрение кинетики разрушения нагруженного образца в рамках обычной модели равнонагруженных цепей 34 161 привело к значительному расхождению теоретических и экспериментальных значений коэффициента у в формуле Журкова. Это расхождение авторы объясняют тем, что в реальном полимере нагрузка на рвущихся цепях значительно превышает среднее значение нагрузки на образец; это не отражается моделью равнонагруженных цепей. [10]
Рассмотрение кинетики реакций изотопного обмена и других реакций с малым выделением свободной энергии, а также протекания каталитических процессов вблизи равновесия, позволило заключить, что при гетерогенном катализе, в противоположность гомогенным реакциям, свободная энергия реакции, как правило, не используется для увеличения концентрации активных частиц. [11]
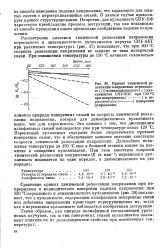 |
Кривые химической релаксации напряжения, перекисно. [12] |
Рассмотрение кинетики химической релаксации напряжения перекисного и диизоцианатного вулканизатов каучука СКУ-8ПГ при различных температурах ( рис. 37) показывает, что при 100 С скорость релаксации напряжения не зависит от типа поперечной связи. [13]
Рассмотрение кинетики накопления кислородсодержащих продуктов на примере окисления циклогексил бензол а позволяет условно выделить несколько участков реакции. [14]
Страницы: 1 2 3 4
