Рассмотрение - механизм - реакция
Cтраница 1
Рассмотрение механизма реакции на поверхности позволяет заключить, что подходящими катализаторами будут, вероятно, окислы переходных металлов и-типа. [1]
Для рассмотрения механизма реакции большое значение имеют данные о состоянии иона меди в катализаторном растворе. Ион Си имеет целиком заполненную Sd-орбиталь и свободные 4s - и 4р - орбитали, разность энергий которых незначительна. Такая электронная структура устойчива при образовании различных координационных соединений. [2]
При рассмотрении механизма реакций с участием кислородных кислот как окислителей прежде всего возникает вопрос, способны ли эти кислоты к простому электронному переходу. Если учесть отрицательный заряд аниона кислородной кислоты, такой переход кажется невозможным. [3]
При рассмотрении механизма реакций диспропорцио-нирования имеется некоторая неопределенность в представлении структуры переходного состояния. [4]
При рассмотрении механизмов реакций ацеталей и кеталей отмечалось, что общий кислотный катализ при гидролизе наблюдается только у ацеталей и кеталей, обладающих определенными структурными особенностями. Обычно же действует специфический кислотный катализ. Представляет интерес вопрос о возможности общего кислотного катализа во внутримолекулярных реакциях, поскольку полагают, что такой катализ проявляется в механизме действия фермента лйзоцима, гидролизующего присутствующие в некоторых полисахаридах йцетадь-ные связи. [5]
При рассмотрении механизма реакции омыления следует обратить внимание на то, что гидрок-сидный ион ( льюисово основание) присоединяется к двойной углерод-кислородной связи, притягиваясь к атому углерода, на котором за счет поляризации имеется небольшой положительный заряд. Несмотря на то что промежуточная переходная частица в этой реакции может содержать две или более гидроксидные или алкоксидные группы, присоединенные к тому или иному атому углерода, такая частица оказывается неустойчивой и от нее отщепляется молекула воды или спирта. [6]
При рассмотрении механизма реакций нуклеофильного присоединения к диацетилену молекулу последнего можно представить двояко: как сопряженную систему тройных связей или как молекулу замещенного ацетилена, в котором одна этинильная группа по отношению к другой, в условиях реакции, является олектроноакцепторным заместителем. [7]
При рассмотрении механизма реакции сульфохлорирования Уол-лшгг [451] допускает, что в противоположность предыдущим млениям реакция ( 3 - 3) обратима. Это предположение основано на том, что сульфохлорирование не происходит в паровой фазе и что полимеризация в системе S02 - олефин, которая протекает по механизму, включающему реакцию типа ( 3 - 3), имеет критическую температуру. Неспособность толуола к сульфохлорированию также объясняется стабильностью бензпльного радикала, вследствие чего равновесие ( 3 - 3) сдвинуто влево. Изобутан не сульфохлорируется в паровой фазе, так как при этом оказывается превышенной критическая температура. [8]
При рассмотрении механизма реакций нуклеофильного присоединения к диацетилену молекулу последнего можно представить двояко: как сопряженную систему тройных связей или как молекулу замещенного ацетилена, в котором одна этинильная группа по отношению к другой, в условиях реакции, является электроноакцепторным заместителем. [9]
При рассмотрении механизма реакций органических соединений с кислородом, идущих при обычной температуре - реакций с а м о о к и с л е-н и я, как темыовых, так и световых, наибольший интерес представляет не столько описание их кинетики с помощью стандартной схемы цепной реакции образующихся радикалов, сколько начальный этап. [10]
При рассмотрении механизма реакций органических соединений с кислородом, идущих при обычной температуре, - реакций самоокисления, как темновых, так и световых, наибольший интерес представляет не столько описание их кинетики с помощью стандартной схемы цепной реакции образующихся радикалов, сколько начальный этап. [11]
 |
УФ-спектры метилэтилке. [12] |
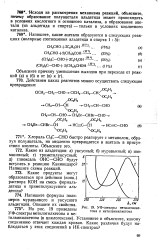
Исходя из рассмотрения механизма реакций, объясните, почему образование полуацеталя альдегида может происходить в условиях кислотного и основного катализа, а образование аце-таля ( из альдегида и спирта) - только в условиях кислотного катализа. [13]
Исходя из рассмотрения механизма реакций, объясните, почему образование полуацеталя альдегида может происходить в условиях кислотного и основного катализа, а образование аце-таля ( из альдегида и спирта) - только в условиях кислотного катализа. [14]
Приступая к рассмотрению механизма конденсационных реакций лигнина, раньше всего необходимо уяснить, что в гомогенной и гетерогенной среде превращения протекают совершенно различными путями. [15]
Страницы: 1 2 3 4