Равновесное межатомное расстояние
Cтраница 3
Для многоатомных молекул, так же как и для двухатомных молекул, модель жесткого ротатора - гармонического осциллятора тождественна предположению о независимости равновесных межатомных расстояний от колебательных и вращательных квантовых чисел, а также предположению об отсутствии ангармоничности колебаний и взаимодействия колебаний и вращения. Кроме того, в рассматриваемом приближении колебания не зависят друг от друга. [31]
 |
Связь между силой и - смещением ( т. е. расстоянием между частицами материала для плоскостей атомов, ограничивающих потенциальную поверхность разрушения. [32] |
Предполагают, что коэффициент концентрации напряжений Ингли-са можно применить к системе, описываемой уравнением ( 31), причем эффективный радиус кривизны в вершине трещины приближается к равновесному межатомному расстоянию Я. Коэффициент концентрации напряжений был получен из модели сплошной среды; для подтверждения возможности применения его к атомистической модели вещества привлекается теория Нейбера, согласно которой вычисляются напряжения в надрезе. [33]
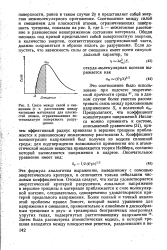
Дальнейшее сближение атомов ( на расстояние, меньшее г) требует больших затрат энергии вследствие взаимного отталкивания одноименно заряженных ядер атомов. Равновесное межатомное расстояние г0 называют длиной химической связи ( d), оно является одной из ее главных характеристик. [34]
 |
Изменение запаса потенциальной энергии Е системы из двух атомов в одорода в зависимости от расстояния г между их центрами. [35] |
Дальнейшее сближение атомов ( на расстояние меньше го) требует больших затрат энергии вследствие взаимного отталкивания одноименно заряженных ядер атомов. Равновесное межатомное расстояние г о называют длиной химической связи d; длина является одной из главных характеристик связи. [36]
Описанные нами методы расчета электронных состояний молекул далеко не всегда дают удовлетворительные результаты, близкие к экспериментальным. Так, например, оказываются завышенными равновесные межатомные расстояния неправильными получаются значения энергии атомизации и силовых постоянных ( см. § 6, гл. [37]
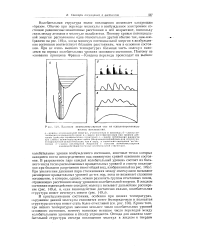 |
Влияние межмолекулярных сил на идеализиропанную полосу поглощения. [38] |
Колебательная структура полос поглощения возникает следующим образом. Обычно при переходе молекулы в возбужденное электронное состояние равновесные межатомные расстояния в ней возрастают, поскольку связь между атомами в молекуле ослабляется. Поэтому кривые потенциальной энергии расположены одна относительно другой обычно так как. При не очень высоких температурах большая часть молекул находится на первых колебательных уровнях основного состояния. [39]
Следует иметь в виду, что численные результаты, полученные таким образом, довольно чувствительны к использованным приближениям. Для того чтобы учесть взаимодействие на расстояниях порядка равновесных межатомных расстояний, для атомов Хе и F использовали атомные орбитали слэтеровского типа. [40]
Как видно из формулы (2.106), величины, обусловливающие ние исходной решетки, являются важными характеристиками структуры жидкости. Можно поэтому сказать, что структура жидкости характеризуется набором равновесных межатомных расстояний, числом атомов на этих расстояниях и размытостью координационных сфер. Вопрос о структурном соответствии распределения атомов в жидком и твердом состояниях вещества решается также при сравнении экспериментальной кривой интенсивности с теоретическими, рассчитанными по заданным моделям. [41]
На фиг, 15 показано, как изменяется с расстоянием rs энергия низшего атомного s - состоя-ния в литии. К преимуществам метода относится и то, что он позволяет вычислить равновесное межатомное расстояние, энергию сцепления и сжимаемость, если допустить, что можно пренебречь всеми вкладами в потенциал решетки, кроме вклада от иона в центре ячейки. [42]
Например, для лития энергия связи в молекуле Li, 1 14 эВ, равновесное межатомное расстояние гравн. Для кристаллической решетки Li энергия решетки Ц 7 эВ, равновесное расстояние между атомами составляет 3 03 А и, формально, при координационном числе кл. [43]
Как известно из теории строения вещества, валентно-химические силы характеризуются потенциальными кривыми, передающими взаимную потенциальную энергию двух атомов, как функцию расстояния между последними. На этих кривых характерной является точка минимума ( дно потенциальной ямы), отвечающая равновесному межатомному расстоянию - длине связи и равновесной энергии диссоциации ( с учетом нулевой энергии) - энергии связи. Потенциальная яма узкая и стенки ее круты. Длины и энергии связей измеряются рентгенострук-турным, электронографическим, спектроскопическим, термохимическим и другими современными физическими методами. Наблюдается далеко идущая аддитивность длин, а также аддитивность энергий связей, что важно для их практического применения. [44]
 |
Относительное расположение синглетных и триплегных п л - и яя - уровней энергии в ряду ароматических альдегидов. [45] |
Страницы: 1 2 3 4