Среднее межатомное расстояние
Cтраница 1
Среднее межатомное расстояние в ct - Zr равно 3 19 А, a fl - Zr - - 3 12 А. На основании правила Юм-Розери следует ожидать, что большинство металлов, используемых в сплавах с цирконием ( Си, Ni, Fe, Mn, Cr, W, Mo, V и др.), атомные диаметры которых 2 4 - 2 9 А, должны растворяться лучше в ft - Zr, чем в a - Zr, и значительно лучше в титане. Это наблюдается в действительности. Растворимость металлов в a - Zr при комнатной температуре не превышает десятых долей процента, вследствие чего они очень мало влияют на температуру a ( 3-превра-щения ( в отличие от титана); повышают температуру перехода только А1 и Sn. Поэтому термическая обработка с целью стабилизации 3-фазы имеет меньшее значение для сплавов циркония, чем для сплавов титана. Например, максимальная растворимость железа в ( 5 - Ti 23 2 атомн. В a - Ti растворяется до 40 % алюминия, а в a - Zr - 7 атомн. [1]
При этом среднее межатомное расстояние Rt не увеличивается, как этого следовало ожидать, а даже несколько I. Сопоставляя температурную зависимость ь он пришел к что при нагревании жидкого металла происходят два взаимно компенсирующих друг друга процесса: с одной стороны, томное расстояние растет за счет увеличения объема, а с оно уменьшается за счет сближения атомов, связанного с шением координационного числа. [2]
 |
Атомная функция распределения. [3] |
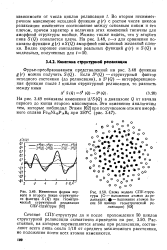
При повышении температуры средние межатомные расстояния в жидкости несколько увеличиваются, а межатомные расстояния в первой координационной сфере изменяются мало. Значительно хуже согласуется координата второго максимума радиальной функции распределения в жидкой фазе с соответствующей координатой в кристалле. [4]
Сопоставляя эти данные со средними межатомными расстояниями ( см. табл. 6), легко увидеть, что оба расстояния в диазогруппе незначительно отличаются от расстояний, вычисленных для связей C N и NN в соответствии с принятым выше строением. [5]
Сопоставляя эти данные со средними межатомными расстояниями ( см. табл. 6), легко увидеть, что оба расстояния в диазогруппе незначительно отличаются от расстояний, вычисленных для связей CN и NN в соответствии с принятым выше строением. [6]
Такое перемещение атомов, превышающее средние межатомные расстояния, называют диффузией. При повышении температуры диффузия ускоряется вследствие увеличения амплитуды колебания атомов кристаллической решетки. [7]
 |
Две конфигурации ( а и ( б первой кЪординационной сферы атома А в модели центральных атомов, обладающие одинаковой энергией центральных атомов А. [8] |
Это приводит к регулярности в расположении атомного окружения со средним межатомным расстоянием порядка атомного диаметра. Следовательно, можно допустить, что каждый атом помещен в собственную ячейку. Поле, действующее на каждый атом в его ячейке, быстро флуктуирует и может быть заменено на среднее поле сферической симметрии. [9]
В отличие от триоктаэдрических структур в А1 - содержа-щих диоктаэдрических структурах значения средних межатомных расстояний А1 - О октаэдров уже не являются постоянными, а заметно отличаются для разных минералов. [10]
 |
Корреляция величин X и N Is в соединениях M ( EDTA Na.| Корреляция величин X и электроотрицательности % для различных атомов М. [11] |
Сдвиг линии лиганда в зависимости от М должен симбатно изменяться с обратной величиной среднего межатомного расстояния металл - лиганд: 1 / гм-лиг. Сравнительно большой размер ионов или атомов Bi, Hg / Pb способствует уменьшению ве г личины г, а тем самым и уменьшению энергий связи лиган-дов. Физически это связано, в частности, с влиянием потенциала Маделунга на сдвиг рентгеноэлектронной линии. [12]
 |
Дифракционная картина от монокристалла.| Дифракционная картина от поликристалла. [13] |
Для получения дифракционной картины существенно, чтобы длина волны используемого излучения была сравнима с этим средним межатомным расстоянием. [14]
Страницы: 1 2 3 4