Раствор - исследуемый - соединение
Cтраница 1
Растворы исследуемых соединений флуоресцируют при 293 К - Переход от неполярных растворителей ( гексан, цикло-гексан, бензол) к полярным ( спирты, диметилформамид) сопровождается батохромным сдвигом ( 5 - 30 нм) и размытием колебательной структуры полосы флуоресценции исследуемых соединений. При этом для соединений 1 - 10 наблюдается увеличение квантовых выходов и времени жизни флуоресценции, а для 11, 12 - тушение флуоресценции. Понижение температуры до 77 К приводит к увеличению интенсивности флуоресценции и появлению долгоживущей фосфоресценции. В спектрах флуоресценции и фосфоресценции замороженных растворов исследуемых соединений проявляется с большой интенсивностью частота 1200 - 1400 см-1. Измерены времена жизни производных 8-оксихинолина при 77 К. Высказаны предположения о механизме их люминесценции. Определены константы равновесий, области рН существования отдельных форм молекул соединений, Ятах и етах полос поглощения этих форм. [1]
Растворы исследуемых соединений флуоресцируют при 293 К. Переход от неполярных растворителей ( гексан, цикло-гексан, бензол) к полярным ( спирты, диметилформамид) сопровождается батохромным сдвигом ( 5 - - 30 нм) и размытием колебательной структуры полосы флуоресценции исследуемых соединений. При этом для соединений 1 - 10 наблюдается увеличение квантовых выходов и времени жизни флуоресценции, а для 11, 12 - тушение флуоресценции. Понижение температуры до 77 К приводит к увеличению интенсивности флуоресценции и появлению долгоживущей фосфоресценции. В спектрах флуоресценции и фосфоресценции замороженных растворов исследуемых соединений проявляется с большой интенсивностью частота 1200 - 1400 см-1. Измерены времена жизни производных 8-оксихинолина при 77 К. Высказаны предположения о механизме их люминесценции. Определены константы равновесий, области рН существования отдельных форм молекул соединений, Ятах и егаах полос поглощения этих форм. [2]
Растворы исследуемых соединений в легком петролейном эфире ( примерно 2 % - ные) наносили при помощи капилляра на слой силикагеля на расстоянии 10 мм от края пластинки ( размер пластинок 13x18 см, поверхность матовая), расстояние между пробами не менее 15 мм. [3]
Из-за высоких диэлектрических констант растворы исследуемых соединений в воде или серной кислоте дают очень плохие сигналы, в связи с чем измерения следует проводить в тонких капиллярах. [4]
Выясняют влияние рН на поглощение раствора исследуемого соединения: а) снимают спектры поглощения растворов, содержащих определяемый элемент и реагент ( взятый без большого избытка) при различных значениях рН ( рис. 18) и определяют Я Т1Г1Х комплекса; б) строят график в координатах А - рН при Ятах комплексного соединения. Максимумы поглощения комплекса и диссоциированной формы реагента часто совпадают. На рис. 19 приведена зависимость А - f ( рН) для комплекса и реагента при Я, соответствующей максимуму поглощения комплекса, и показано рНопт, при котором комплекс уже образовался в максимальной степени, а поглощение реагента сказывается на суммарной оптической плотности в наименьшей степени. [5]
Методика требует приготовления большого числа растворов исследуемого соединения и работы с достаточно концентрированными буферными растворами. Одновременное определение оптической плотности и величины рН раствора невозможно. Зависимость оптической плотности от рН дискретна, а увеличение числа экспериментальных точек связано с большим расходом веществ и затратами труда. [6]
Можно также налить в сосуд 3 раствор исследуемого соединения до надлежащей высоты, а в сосуд К поместить 5 % - ный раствор йодистого калия. [7]
 |
Схема прохождения луча света через призму Николя и вращение плоскости поляризованного света оптически активным веществом. [8] |
Если при пропускании такого луча сквозь раствор исследуемого соединения произойдет отклонение его плоскости поляризации от первоначальной на определенную величину угла, измеряемую в градусах, то такое вещество оптически активно. Оптическая активность большинства органических соединений связана со строением их молекул, что подтверждается фактом оптической активности их растворов. Связь между строением органических веществ и их оптической активностью видна из следующих примеров. [9]
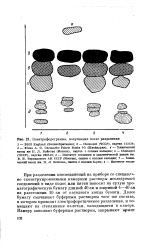 |
Электрофореграмма, полученная после разделения. [10] |
При разделении азосоединений на приборе со специально сконструированными камерами растворы исследуемых соединений в виде полос или пятен наносят на сухую хро-матографическуго бумагу длиной 40 см и шириной 4 - 40 см на расстоянии 10 см от катодного конца бумаги. Далее бумагу смачивают буферным раствором того же состава, в котором проводят электрофоретическое разделение, и помещают на стеклянные палочки, находящиеся в камере. [11]
 |
Электрофореграмма, полученная поело разделения. [12] |
При разделении азосоединений на приборе со специально сконструированными камерами растворы исследуемых соединений в виде полос или пятен наносят на сухую хро-матографическую бумагу длиной 40 см и шириной 4 - 40 см на расстоянии 10 см от катодного конца бумаги. Далее бумагу смачивают буферным раствором того же состава, в котором проводят электрофоретическое разделение, и помещают на стеклянные палочки, находящиеся в камере. [13]
 |
Обработка фронтальной выходной кривой. [14] |
Для определения емкости колонки обычно проводят франтальную хром атографию раствором исследуемого соединения до тех пор, пока концентрация его в элюате не станет равной концентрации в исходном растворе. После этого хроматогра-фирование прекращают и колонку промывают элюентом, который замещает исходный раствор в свободном объеме колонки, не смывая вещества, удерживаемого неподвижной фазой. Когда концентрация вещества в элюате снизится ниже предела обнаружения, элюент заменяют на раствор, который вымывает вещество с неподвижной фазы, и злюируют его полностью. Определение концентрации вещества в этом элюате позволяет определить количество соединения, первоначально удерживаемого колонкой. [15]
Страницы: 1 2 3