Раствор - слабая кислота
Cтраница 2
В растворах слабых кислот и щелочей эти величины определяют иначе. [16]
В растворах слабых кислот и щелочей наблюдается расхождение между концентрацией активных ионов Н и ОН и концентрацией потенциальных. [17]
В растворах слабых кислот ( борная, винная, лимонная) и их солей оксидная пленка не растворяется. В этом случае получают беспористые, плотные, не проводящие электрический ток покрытия толщиной до 1 мкм. Такие пленки используют в качестве электроизоляционных покрытий в производстве конденсаторов. [18]
В растворах слабых кислот или слабых оснований в результате взаимодействия образуются гидролизующиеся соли. В этом случае процесс нейтрализации заметно обратим. [19]
При титровании раствора слабой кислоты рабочим раствором сильного основания получается соль, имеющая щелочную реакцию вследствие гидролиза. Более точная характеристика получается путем вычисления рН в точке эквивалентности. [20]
Рассмотрение свойств растворов слабых кислот и оснований как в присутствии, так и в отсутствие их солей преследовало цель показать общие приемы, которыми необходимо пользоваться при решении конкретных задач. Встречавшиеся по ходу дела формулы не следует запоминать. [21]
При титровании раствора слабой кислоты рабочим раствором сильного основания получается соль, имеющая щелочную реакцию вследствие гидролиза. Более точная характеристика получается путем вычисления рН в точке эквивалентности. [22]
Кривые рефракции растворов слабых кислот не проходят через максимум. Чем ниже константа диссоциации, тем меньше угол наклона кривой ( прямой), приближающейся к горизонтали. [23]
Если к раствору слабой кислоты добавлена соль этой кислоты и сильного основания, которая хорошо диссоциирует на ионы, то диссоциация. [24]
Если к раствору слабой кислоты прибавить ее соль, происходит значительное уменьшение степени диссоциации кислоты. Пусть, например, в 0 1 М раствор уксусной кислоты СН3СООН ( а1 3 %) внесен 0 1 М раствор ацетата натрия, в котором эта соль полностью диссоциирована. [25]
Если к раствору слабой кислоты прибавляется нейтральная соль, то ионы последней являются главным фактором, определяющим ионную силу раствора. Если же, с другой стороны, измерения производятся в буферном растворе ( например, уксусная кислота - f - ацетат натрия), то ионная сила раствора зависит от состава самого буфера, и в этом случае могут получиться значительные вторичные солевые эффекты даже без прибавления других солей. Согласно классической теории диссоциации, концентрация ионов водорода в буфер-ном растворе уксусной кислоты - - ацетат натрия зависит только от соотношения составных частей буфера. [26]
Если к раствору слабой кислоты прибавить ее соль, то происходит значительное изменение ( уменьшение) степени диссоциации кислоты. Допустим, в раствор уксусной кислоты СН3СООН ( ее степень диссоциации в 0 1 М растворе 1 3 %) внесен ацетат натрия CH3COONa, полностью диссоциирующий. [27]
Если к раствору слабой кислоты добавлена соль этой кислоты и сильного основания, которая хорошо диссоциирует на ионы, то диссоциация кислоты подавляется и концентрацию молекул СНзСООН можно считать в первом приближении равной концентрации всей находящейся в растворе уксусной кислоты. С другой стороны, поскольку соль CH3COONa является сильным электролитом, концентрацию ионов СНзСОО можно считать равной концентрации всей растворенной соли. [28]
Если к раствору слабой кислоты прибавить ее соль, происходит значительное уменьшение степени диссоциации кислоты. [29]
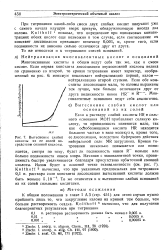 |
Вытеснение слабой кислоты из ее солей посредством соляной кислоты. [30] |
Страницы: 1 2 3 4