Раствор - комплекс
Cтраница 1
Раствор комплекса, содержащего Мп3, имеет фиолетовую окраску; титрант стандартизуют по 0 1 М раствору соли Мора. [1]
Раствор комплекса в пиридине используется для окисления веществ, содержащих группировки, чувствительные к кислотам. [2]
Растворы комплексов в хлороформе проводят электрический ток. Аминокомплексы хлорборанов - кристаллические вещества, обычно легкоплавкие. Все они хорошо растворимы в воде, причем растворение идет без разложения. Гидролизуются они лишь при длительном нагревании до 150 С в запаянной трубке. Стойки к действию кислот, но разлагаются щелочами. При этом образуются ионы гидроксиборгидридов [ НВ ( ОН) 4 - п ] - и выделяется амин. [3]
Растворы комплекса в ледяной уксусной кислоте не изменяют люминесцентных свойств в течение недели. Температура опыта должна быть постоянной, так как повышение ее уменьшает интенсивность люминесценции. [4]
Растворы комплекса окрашиваются очень быстро и устойчивы в течение нескольких часов. Метод позволяет определять десятитысячные доли процента титана и более. Железо ( III) восстанавливают аскорбиновой кислотой. [5]
Растворы комплексов сохраняют для проведения других опытов. [6]
Раствор комплекса был получен при пропускании сухой двуокиси серы в безводный раствор йода в толуоле до обесцвечивания пробы после добавления воды. [7]
Раствор комплекса в пиридине используется для окисления веществ, содержащих группировки, чувствительные к кислотам. [8]
Растворы комплексов Fe ( II) стабильны только в течение 5 мин. [9]
Растворы комплексов те-трафенилендиамина с галогенсодержащими хинонами имеют глубокую синюю окраску в ацетонитриле или в смесях вода - метанол, однако они почти бесцветны в бензоле или диоксане. Найдено, что комплекс - хлоранила в ацетонитриле проводит ток. Молярная электропроводность комплекса - хлоранила увеличивается при разбавлении. [10]
Раствор комплекса мурексида ( пурпурата аммония) с кальцием окрашен в красный цвет, свободная форма индикатора - в фиолетовый. [11]
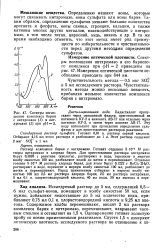 |
Спектры поглощения комплекса бария с нитхромазо ( 1 и нитхромазо ( 2 при рН 2. [12] |
Раствор комплекса бария с нитхромазо. Готовят отдельно 5 - Ю 3 М растворы нитхромазо и хлорида бария. Для приготовления раствора нитхромазо берут 0 3893 г реактива ( кислоты), растворяют в воде, переносят в мерную колбу емкостью 100 мл, разбавляют водой до метки и перемешивают. Отдельно готовят 5 - Ю 3 М раствор хлорида бария, для этого берут 0 1222 г ВаС12 - 2Н2О, растворяют в воде, переносят в мерную колбу емкостью 100 мл, разбавляют до метки и перемешивают. [13]
Растворы комплекса плутония ( IV) с трибутилфосфатом подчиняются закону Бера в пределах исследованных концентраций Pu ( IV) 0 05 - 1 5мг / мл. [14]
Растворы титанониобиевых комплексов неустойчивы и при комнатной температуре медленно разлагаются, вначале с образованием двойного сульфата титана ( l H4) 2TiO ( S04) 2, а затем ниобиевой фазы сложного состава. [15]
Страницы: 1 2 3 4