Раствор - комплекс
Cтраница 3
К раствору комплекса 2 ( 1.72 г, 2.5 ммоль) в 50 мл ацетона добавляют 0.66 г свежеперегнанного дихлордиме-тилсульфида ( 5 ммоль) и нагревают 4 часа. Полученную реакционную массу охлаждают льдом, разбавляют ледяной водой и оставляют на ночь для завершения формирования осадка. Осадок отфильтровывают, сушат на воздухе и перекристал-лизовывают из уксусной кислоты. [31]
Реакция структурирования растворов комплексов претерпевает качественное превращение исходных компонентов. [32]
 |
Константы кислотной диссоциации гидридных комплексов металлов. [33] |
Определено титрованием раствора комплекса основанием. [34]
Оптическая плотность раствора комплекса зависит от температуры. Однако при одновременном измерении оптической плотности анализируемого и стандартного растворов изменение температуры сказывается на точности измерений незначительно. [35]
Кривая светопоглощения раствора комплекса азометина Н с Н3ВО3 имеет пологий максимум в области 415 нм. Оптическая плотность растворов пропорциональна концентрации бора в пределах 2 - 10 мкг В на 100 мл. [36]
Максимальная окраска раствора комплекса развивается в течение 20 мин. Содержание AI, Си, Fe, Ni, Cr и других элементов не должно превышать 0 1 - 20 мкг / мл. Рекомендуется отделение посторонних примесей 8-оксихинолиновым методом. [37]
Зависимость светопоглощения растворов комплексов от температуры, рН и концентрации реагирующих компонентов при постоянной длине волны изучена на примере более чем 50 соединений. Выбранная длина волны соответствует наибольшей разнице между светопоглощением комплексов и реагентов. При увеличении рН на 1 - 2 единицы от рНопт в менее кислую область светопоглощение падает на 30 - 50 % и более. Аналогичное смещение кривых D - рН наблюдается при пропорциональном увеличении концентраций реагирующих компонентов. [38]
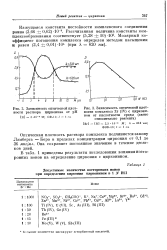 |
Зависимость оптической плотности раствора цирконина от рН.| Зависимость оптической плотности комплекса Zr ( IV с циркони-ном от кислотности среды ( снято относительно реагента. [39] |
Оптическая плотность раствора комплекса подчиняется закону Ламберта - Бера в пределах концентрации циркония от 0 1 до 36 мкг / мл. Она сохраняет постоянное значение в течение десятков дней. [40]
Максимум светопоглощения раствора комплекса находится при 450 ммк. При концентрации Н2О2 выше 0 09 % окраска изменяется из красно-коричневой в желтую. [41]
Максимальная окраска раствора комплекса развивается в течение 20 мин. Содержание Al, Cu, Fe, Ni, Cr и других элементов не должно превышать 0 1 - 20 мкг / мл. Рекомендуется отделение посторонних примесей 8-оксихинолиновым методом. [42]
Электрическая проводимость растворов комплексов PtCl4 - 6NH3; PtCl4 - 5NH3; PtCU - 4NH3; PtCl4 - 3NH3; PtCl4 - 2NH3; K2PtCls - NH3; K2PtCle уменьшается, достигая нуля для PtCUX X2NH3, и затем снова возрастает. Зная, что электрическая проводимость прямо пропорциональна числу ионов, на которые диссоциирует электролит, и что координационное число Pt в этих комплексах равно 6, напишите их координационные формулы. [43]
Оптическая плотность раствора комплекса пропорциональна его концентрации. [44]
Реакция структурирования растворов комплексов претерпевает качественное превращение исходных компонентов. [45]
Страницы: 1 2 3 4