Раствор - металл
Cтраница 2
Теория растворов металлов [37, 43, 102, 111, 173] и растворов расплавленных солей [23, 86, 116, 136] еще не дает возможности рассчитать значения термодинамических функций для реального раствора, исходя из термодинамических свойств чистых компонентов. Такие расчеты зависят от принятой модели раствора, а эта модель, в свою очередь, должна быть построена на основании надежных экспериментальных данных о структуре и термодинамических свойствах большого числа растворов. [16]
Природа растворов металлов в расплавах солей до сих пор остается не вполне ясной и дискуссионной. [17]
Теория растворов металлов [37, 43, 102, 111, 173] и растворов расплавленных солей [23, 86, 116, 136] еще не дает возможности рассчитать значения термодинамических функций для реального раствора, исходя из термодинамических свойств чистых компонентов. Такие расчеты зависят от принятой модели раствора, а эта модель, в свою очередь, должна быть построена на основании надежных экспериментальных данных о структуре и термодинамических свойствах большого числа растворов. [18]
Восстановление растворами металлов можно осуществить в присутствии краун-эфиров, которые солюбилизируют металлы. [19]
Восстановление растворами металлов рассматривается как нуклео-фильный процесс ( см. стр. Обсуждаемый тип восстановления, состоящий в абсорбции водорода олефинами на поверхности переходного металла, является гемолитическим процессом; по-видимому, из металла водород абсорбируется олефинами в виде атомов. [20]
Перевод в раствор металлов - цинка и свинца - раньше их окислов неосуществим ни слабокислыми, ни слабощелочными реагентами, так как в первых окислы растворяются за счет водородных ионов, во вторых - за счет гидроксильных ионов. [21]
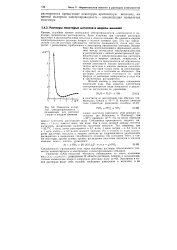 |
Изменение молярной электропроводности с разведением для раствора натрия в жидком аммиаке. [22] |
Однако проводимость растворов металлов в жидком аммиаке настолько велика, что одни только ионы ( и комплексные, и простые) не в состоянии ее обеспечить. Эти растворы значительно отличаются по своей природе от растворов электролитов в воде или в органических растворителях. [23]
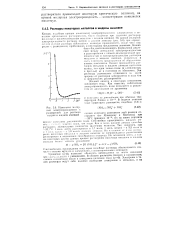 |
Изменение молярной электропроводности с разведением для раствора натрия в жидком аммиаке. [24] |
Однако проводимость растворов металлов в жидком аммиаке настолько велика, что одни только ионы ( и комплексные, и прос i ые) не в состоянии ее обеспечить. Эти растворы значительно отличаются по своей природе от растворов электролитов в воде или в органических растворителях. [25]
Восстановление ацетилена раствором металла ( обычно натрия или лития) в жидком аммиаке дает чистые тракс-олефины. Этот процесс сравним с восстановлением Берча ( стр. [26]
Восстановление ацетилена раствором металла ( обычно натрия или лития) в жидком аммиаке дает чистые трякс-олефины. Этот процесс сравним с восстановлением Берча ( стр. [27]
Различие между растворами металлов в расплавленных солях и жидкими полупроводниками в основном условное. Все разграничения между указанными растворами и системами, обычно относимыми к жидким полупроводникам, можно свести к разнице в степенях ионизации этих систем. [28]
Реакция восстановления растворами металлов в жидком аммиаке относится к числу реакций, для которых тщательный выбор условий и строгий контроль за их соблюдением являются важными факторами, позволяющими провести восстановление с достаточной скоростью и в желаемом направлении. [29]
После погружения в раствор металла распад роданида заметно возрастает, особенно при повышенных температурах. Так, при 90 уже через три часа после начала коррозии роданид не обнаруживается. В присутствии индола распад роданида значительно тормозится. При 90 даже через 9 часов после начала коррозии сохраняется еще около 50 % роданида. [30]
Страницы: 1 2 3 4