Раствор - плутоний
Cтраница 1
Растворы плутония ( V) легче получить добавлением КРиО2СО3 ( тв) к разбавленной кислоте, но водный PuOJiaq) затем диспропорционирует. [1]
Раствор плутония в разбавленной азотной кислоте восстанавливают гидразином до Pu ( III) и осаждают аммиаком светло-лиловый осадок Ри ( ОН) 3, который быстро окисляется до Ри ( ОН) 4 зеленого цвета. Мелкодисперсный осадок гидроксида плутония ( IV) для удаления аммиака промывают водой до начала пептизации. Водную суспензию нагревают до 90 С и пропуска-ют через нее кислород, содержащий Оз, до тех пор, пока окраска не станет золотисто-красной. Осадок центрифугируют, промывают водой и сушат в ва-жууме при 130 С. [2]
Растворы плутония ( III) в обычных кислотах окрашены в темносиний цвет. [3]
Раствор плутония, выходящий из колонны I, и раствор урана, выходящий из колонны III, недостаточно очищены от активности, обусловленной продуктами деления. [4]
Раствор плутония в азотной кислоте концентрируется, затем подвергается денитрации и превращается в сухой порошок РиОг. Для полной очистки уранового продукта используются два-три дополнительных цикла экстракции органическим растворителем. [5]
Раствор плутония в серной кислоте, содержащий железо и уран, предварительно восстанавливали при нагревании сернистым газом, затем удаляли SC2 пропусканием инертного газа и титровали сначала при комнатной температуре, а затем при 70 С. На первой стадии плутоний окисляется до четырехвалентного, железо до трехвалентного и уран до шестивалентного состояния. На второй стадии титруется лишь плутоний до шестивалентного состояния. [6]
Раствор плутония, не содержащий сульфат - и фосфат-ионов, сначала сильно нагревают для удаления легколетучих кислот. HNOs, и выпаривают возможно быстрее до объема 100 - 150 нл. Было показано, что при малой скорости выпаривания микроколичества плутония окисляются только частично или не окисляются совсем. Операция выпаривания должна быть закончена в 20 сек. Кипения раствора необходимо избегать. Полученный раствор РиС22 титруют 0 05 - 0 01 N раствором соли Мора. Конец бюретки и электроды не должны касаться стенок микроконуса во избежание захвата жидкости. [7]
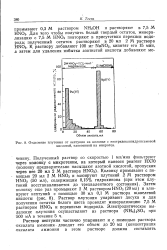 |
Отделение плутония от нептуния на колонке с неотридекангидроксамовой кислотой, нанесенной на микротен. [8] |
Раствор плутония упаривают досуха и для получения остатка белого цвета проводят минерализацию 7 5 М раствором HNO3 и перекисью водорода. [9]
Обработка растворов плутония ( III), осадков гидроокиси Ри ( ОН) 3 концентрированной азотной кислотой при нагревании приводит к почти мгновенному окислению Pu ( III) в четырехвалентное состояние. [10]
Обработкой растворов плутония ( VI) йодистым калием при рН - 2 можно быстро получить Pu ( V) ( см. стр. В более кислых средах одновременно с появлением значительных количеств Pu ( V) начинается его диспропорционирование, и, по всей вероятности, именно этот процесс определяет скорость восстановления Pu ( VI) до Pu ( III), так как реакция Pu ( VI) - Pu ( V) очень быстрая [ 3, стр. [11]
Нагревание растворов плутония ( III) уменьшает его устойчивость. Это особенно заметно в растворах азотной и серной кислот. В оксалатных и карбонатных растворах плутоний ( III) неустойчив, и окисление его наблюдается уж через несколько часов. [12]
Устойчивость растворов плутония ( IV) зависит от комплексующей способности аниона. В 0 5 М Й25О4 Pu ( IV) не изменяет валентности в течение длительного времени. С уменьшением концентрации водородных ионов все большую роль начинают играть реакции диспропорционирования, и количества других валентных форм плутония при постоянной кислотности увеличиваются в ряду НМОз-НС1-НС1О4. [13]
Светопоглощение растворов плутония не изменяется в течение длительного времени при условии, конечно, сохранения данного валентного состояния. [14]
Объемы растворов плутония определяли измерительными капиллярами, а для титрования служили микро-бюретки с точи остью отсчета 0 8 нл. [15]
Страницы: 1 2 3 4