Раствор - плутоний
Cтраница 3
 |
Восстановление Pu ( VI под действием собственного а-излучения в зависимости от времени. [31] |
Методы электролитического получения растворов плутония в каком-либо одном валентном состоянии находят все более широкое применение как в препаративной химии, так и в электрометрическом анализе. [32]
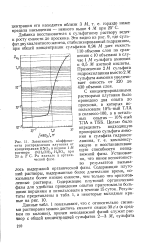 |
Зависимость коэффициента распределения плутония от концентрации HNO., в водном 1 М растворе ( NH2OH 2 - H SO4 при 23 2 С. Ри вначале в органической фазе. [33] |
С концентрированными: растворами плутония была проведено два опыта до; проскока, в которых использовали 10 % - ный ТЛА в солвессо-100, а в остальных опытах - 10 % - ный: ТЛА в ТББ. [34]
Азотнокислый или солянокислый - раствор плутония ( IV) ( оптимальная концентрация плутония - 1 мг / мл) не содержащий мешающих катионов и комплексующих анионов, нагревают до кипения для удаления СОз. К раствору по каплям прибавляют 20 % - ный раствор МН4ОН без ( СОг) при постоянном перемешивании до запаха аммиака. Раствор с осадком нагревают в течение 3 - 5 мин. Затем добавляют небольшой избыток раствора NH4OH, оставляют стоять в течение 5 - 10 мин. Осадок промывают 2 - 3 раза водой, подшелаченной несколькими каплями 20 % - ного аммиака. Фильтр с осадком переносят в платиновый тигель и высушивают на электрической плитке. Затем его прокаливают при 1000 С в течение 2 - 3 час. [35]
Для полного выделения из растворов плутония в различных валентных состояниях необходимо предварительное переведение плутония в четырехвалентное состояние. [36]
При равном содержании в растворе плутония и урана для полного отделения урана достаточно провести одно осаждение, при большем содержании урана требуется повторное осаждение. Методика осаждения описана на стр. [37]
Помещают 8 - 10 мл раствора плутония в 1 М НС1О4 ( в качестве среды) в ячейку, для удаления кислорода пропускают гелий при перемешивании мешалкой. Затем устанавливают ноль интегратора и окисляют при потенциале 0 435 в относительно того же электрода до автоматической остановки процесса. Измеряют показание интегратора и вычисляют количество плутония. [38]
 |
Константы гидролиза плутонил-иона. [39] |
Краус и Дэм [89] титровали щелочью раствор плутония ( V), не содержащий СОа. Полученные результаты приведены в табя. [40]
Это вещество быстро образуется при нагревании растворов плутония ( IV) с низкой кислотностью и более медленно в случае выдержки этих растворов при комнатной температуре. Плутониевый полимер медленно разрушается сильно концентрированной кислотой при комнатной температуре и быстрее - при 90 С. Так как плутониевый полимер не экстрагируется, то в процессах разделения необходимо избегать условий, способствующих его образованию. Присутствие агентов, комплексующих Ри4, замедляет образование полимера и ускоряет его разрушение. [41]
Электрохимические методы особенно удобны для приготовления растворов плутония и других элементов в определенном валентном состоянии. Получение нужного валентного состояния при этом достигается без добавления посторонних веществ. Эти методы в настоящее время являются широко распространенными приемами, используемыми в аналитической и препаративной химии. [42]
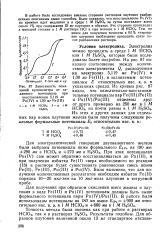 |
Зависимость показаний кулонометра от за. [43] |
В работе было исследовано влияние старения растворов плутония разбавленных описанным выше способом. Было показано, что восстановление Pu ( VI) во времени идет медленно и в среде 1 М FLSCU за сутки составляет всего около 1 % при содержании 25 мг плутония в образце. [44]
Таким образом, при работе с растворами плутония ( IV), находящимся хотя бы частично в виде полимера, возникают трудности, которые могут быть преодолены только путем полной деполимеризации. [45]
Страницы: 1 2 3 4