Раствор - соль - цирконий
Cтраница 1
Раствор соли циркония: 0 265 г ZrOCl2 8Н2О или 0 220 г Zr ( NO3) 4 2Н2О растворяют в 50 мл воды, добавляют 700 мл НС1 ( плотность 1 19 г / см3) и разбавляют водой до литра. Целесообразно приготовить запасной раствор соли циркония, определить концентрацию последнего осаждением аммиаком и применять для приготовления реактива по мере надобности. Смешивать заранее раствор I и раствор II нельзя, так как при хранении образуется осадок. [1]
Раствор соли циркония после стояния в течение нескольких месяцев может стать мутным. Поэтому надо применять свежеприготовленные растворы или часто устанавливать их титр. [2]
Растворы соли циркония в 1 М НС1 имеют частично коллоидную природу, а 0 1 М водный раствор нитрата циркония является коллоидным. Это свойство нитрата циркония было использовано Айресом [326] для ионообменного метода очистки циркония от примесей. [3]
Гидролиз растворов солей циркония в большинстве случаев, даже при нагревании, не приводит к образованию осадков и только в нитратных растворах наблюдаются появление опалесценции и частичное выпадение циркония в осадок. При гидролизе равновесие устанавливается крайне медленно. При гидролизе возможно образование иона цирконила, но, как и в случае титанила, нет прямых доказательств присутствия или отсутствия его в растворах. [4]
К раствору соли циркония ( хлорида или нитрата) добавляют несколько капель ализаринсульфоната натрия. При этом образуется раствор циркон-ализаринового лака красного цвета. При добавлении F - красная окраска исчезает. [5]
К раствору соли циркония прибавляют от 1 до 5 г хлорида аммония, нагревают до 70 - 80 С и прибавляют разбавленный раствор аммиака в небольшом избытке. При небольшом содержании циркония раствор с осадком оставляют на некоторое время на теплой бане для лучшей коагуляции. Осадок промывают на фильтре 3 - 4 раза 2 % - ным раствором хлорида или нитрата аммония. Фильтр с осадком озоляют в платиновом тигле, а затем прокаливают при 1000 - 1200 С до постоянного веса. [6]
В растворах солей циркония могут существовать одновременно бесцветные ионы Zr4, ионы цирконила ZrO2 и различные полимеризованные ионы. Степень полимеризации увеличивается с повышением концентрации соли циркония и зависит от кислотности раствора. При введении Н2р2 полимеризация ионов циркония снижается. [7]
При добавлении к растворам соли циркония в 0 08 - 0 1 N НС1 водного раствора арсеназо I розовая окраска реагента переходит в фиолетовую. Кроме циркония, при таком рН с арсеназо взаимодействуют титан и гафний. Мешают ионы SO42, а также фториды, фосфаты, органические онсикислоты и др. Мешают большие количества тория и урана. [8]
Большинство исследований процесса полимеризации растворов солей циркония имеет качественный характер. Работы по определению факторов полимеризации в различных условиях пока еще немногочисленны. [9]
В лаборатории имеются два раствора соли циркония. [10]
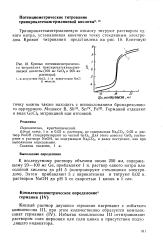 |
Кривые потенциометрическо-го титрования трипирокатехингерманиевой кислоты ( 100 мг GeO2 в 200 мл раствора. [11] |
Избыток комплексона III оттитровывают раствором соли циркония или соли цинка в присутствии подхо дящего индикатора. [12]
Отбирают 15 мл аликвотной части раствора соли циркония, содержащие 14 мг циркония, в коническую колбу для титрования, разбавляют водой до 100 мл, прибавляют 0 5 мл 0 1 % - ного раствора ксиленолового оранжевого и титруют при рН 1 0 01 М раствором трилона Б до перехода малиновой окраски в желтую. Перед концом титрования раствор трилона Б прибавляют медленно, по каплям, и тщательно перемешивают. Окраску титруемого раствора сравнивают со свидетелем, представляющим собой предыдущую перетит-рованкую пробу. [13]
Раствор комплексона III стандартизируют по раствору соли циркония. Аналогично титруется и гафний. Количество гафния должно быть учтено при стандартизации и титровании пробы. [14]
Титр устанавливают по нормали или раствору соли циркония. [15]
Страницы: 1 2 3 4