Атермальный раствор
Cтраница 1
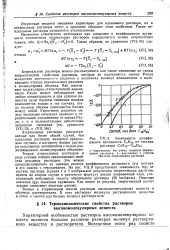 |
Зависимость коэффициента активности С7Н16 от состава раствора С7Н16 - С16Н34. [1] |
Атермальные растворы можно рассматривать как такие идеальные по своим энергетическим свойствам растворы, которые не подчиняются закону Рауля вследствие значительного различия в величинах молекул компонентов и вытекающего отсюда значительного различия в молекулярных объемах. Как показывает молекулярно-статистический анализ, закон Рауля может соблюдаться при любых концентрациях и при условии равенства нулю теплоты смешения жидких компонентов только в тех случаях, когда мольные объемы компонентов близки между собой. [2]
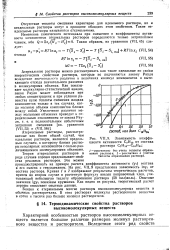 |
Зависимость коэффициента активности С7Н16 от состава раствора С7Н16 - С16Н34. [3] |
Атермальные растворы, рассматриваемые как более общий случай, чем идеальные растворы, являются предельным случаем, к которому близки растворы неполярных компонентов с сильно различающимися молекулярными объемами. [4]
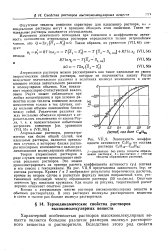 |
Зависимость коэффициента активности С7Н16 от состава раствора С7Н16 - CieH34. [5] |
Атермальные растворы можно рассматривать как такие идеальные по своим энергетическим свойствам растворы, которые не подчиняются закону Рауля вследствие значительного различия в величинах молекул компонентов и вытекающего отсюда значительного различия в молекулярных объемах. Как показывает молекулярно-статистический анализ, закон Рауля может соблюдаться при любых концентрациях и при условии равенства нулю теплоты смешения жидких компонентов только в тех случаях, когда мольные объемы компонентов близки между собой. [6]
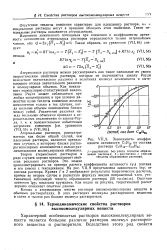 |
Зависимость коэффициента активности С7Н16 от состава раствора С7Н16 - CieH34. [7] |
Атермальные растворы, рассматриваемые как более общий случай, чем идеальные растворы, являются предельным случаем, к которому близки растворы неполярных компонентов с сильно различающимися молекулярными объемами. [8]
Атермальные растворы обычно характеризуются малыми значениями Н, которые в пределе можно положить равными нулю. Такое поведение часто характерно для растворов полимерных молекул в низкомолекулярных растворителях. [9]
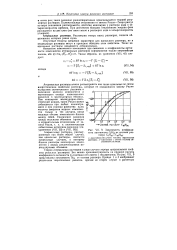 |
Зависимость коэффициента активности QHje от состава раствора C7Hle - CieH34. / - рассчитано без учета теплоты образования раствора. 2-рассчитано с учетом теплоты образования раствора. [10] |
Атермальные растворы можно рассматривать как такие идеальные по своим энергетическим свойствам растворы, которые не подчиняются закону Рауля вследствие значительного различия в величинах молекул компонентов и вытекающего отсюда значительного различия в молекулярных объемах. Как показывает молекуляр но-статистический анализ, закон Рауля может соблюдаться при любых концентрациях и при условии равенства нулю теплоты смешения жидких компонентов только в тех случаях, когда мольные объемы компонентов близки между собой. [11]
Теория атермальных растворов в ряде случаев хорошо предсказывает свойства реальных растворов. Это можно проиллюстрировать на примере расчета коэффициента активности ( YI) гептана в его смесях с гексадеканом. На рис. VII, 9 представлена зависимость Inyi от состава раствора. Опытные значения Igyi показаны кружками. Как видно из рисунка, теоретический расчет хорошо описывает опытные данные. [12]
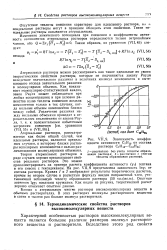 |
Зависимость коэффициента активности С7Н16 от состава раствора С7Н16 - CieH34. [13] |
Теория атермальных растворов в ряде случаев хорошо предсказывает свойства реальных растворов. [14]
Теория атермальных растворов в ряде случаев хорошо предсказывает свойства реальных растворов. Это можно проиллюстрировать на примере расчета коэффициента активности ( ft) гептана в его смесях с гексадеканом. На рис. VII, 9 представлена зависимость Irrfi от состава раствора. [15]
Страницы: 1 2 3 4