Контактный раствор
Cтраница 1
 |
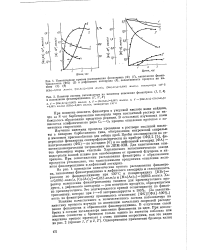
Кривая зажигания искры для хо лодных медных контактов. [1] |
Контактный раствор ( или зазор) - это расстояние, которое образуется между контактными поверхностями при их полном расхождении. Расхождение контактов, как правило, связано с возникновением электрических разрядов в виде искры или дуги. Кроме того, искры и дуги сильно сокращают срок службы контактов и поэтому обычно принимают меры для предотвращения их образования или меры по уменьшению их вредного действия. [2]
 |
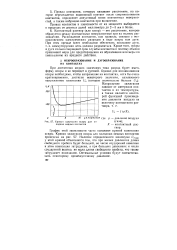
Зависимость скорости образования ВА. [3] |
Увеличение кислотности контактного раствора уменьшает скорости образования ХВА и ВА. [4]
Добавление двухвалентной меди в контактный раствор синтеза хлорэтена ( CuCl - NH4C1 - НС1) приводит к появлению [97] в продуктах дихлорэтенов и уменьшению выхода хлорэтена. Очевидно, их образование происходит через одно и то же промежуточное соединение, которым может быть хлорвинилмедь. Протолиз этого соединения приводит к образованию хлорэтена, а взаимодействие с СиСЬ - хлорвинилкуприхлорида. Пока неясно, является ли превращение р-хлорвинилмеди в р-хлорвинил-куприхлорид результатом реакции замещения или переноса электронов от Си к Си2 через хлоридные мостики. [5]
В колбу для титрования вносят 1 мл контактного раствора, разбавляют его в несколько раз водой и титруют раствором НС1 известной концентрации ( 0 2 М) в присутствии метилоранжа. [6]
В табл. 4 представлена зависимость значения рН контактного раствора от величины т: ж и рН исходного раствора. При этом, согласно данным табл. 3, опыты проводились при условиях ( величина т: ж и рН исходного раствора), гарантирующих полноту очистки раствора от ионов хрома. [7]
Для гашения дуги наиболее часто применяются следующие конструктивные меры: увеличение контактного раствора и увеличение скорости расхождения контактов; применение дугогася-щих камер и деионных решеток; искусственное увеличение скорости движения дуги и ее длины с помощью магнитного дутья. [8]
Описываемый хроматографический метод позволяет осуществить анализ продуктов реакции, содержащихся в контактном растворе, без их предварительного выделения. [9]
Как показывают проведенные исследования, скорость установления окислительно-восстановительного равновесия реакции ( 1) в контактном растворе зависит от диффузии ионов Си ( II) к поверхности и от поверхности металлической меди, а ионы Си ( II) в гомогенной фазе находятся в равновесии с адсорбированной фазой. [11]
При попытке окислить фенантрен в уксусной кислоте нами найдено, что за 8 час барботирования кислорода через контактный раствор не наблюдалось образования продуктов реакции. [13]
Во избежание полимеризации растворенного кремнезема его содержание следует определять сразу же после отделения твердой фазы, не оставляя контактный раствор на длительное время. [14]
Интересно отметить, что в процессе сорбции из щелочных растворов наблюдается не свойственное анионному обмену уменьшение значения рН контактных растворов ( табл. 1), которое может быть обусловлено преимущественной сорбцией ионов щелочного металла в этих условиях. [15]
Страницы: 1 2 3