Титрующий раствор
Cтраница 1
Титрующий раствор приливают из микробюреток емкостью от 0 1 до 2 мл со съемным кончиком. Последнее необходимо, так как кончик наиболее подвержен загрязнениям и легко ломается. При титровании кончик микробюретки погружают в титруемый раствор, а титрующий подают, поворачивая винт затвора. [1]
Титрующий раствор прибавляется из калиброванной микробюретки на 5 - 10 мл, пришлифованной к склянке из темного, стекла или покрашенной темной краской. [2]
Титрующий раствор, приливаемый из бюретки, добавляют в химически эквивалентном количестве. Когда количество прибавленного вещества химически эквивалентно количеству определяемого вещества, говорят, что достигнута точка эквивалентности. [3]
Добавляют титрующий раствор при помощи бюретки из сосуда ( см. выше), отмечая отклонения гальванометра и соответствующий объем по циферблату бюретки, время от времени проверяя расположение аппаратуры под микроскопом и выдвигая, по мере увеличения объема, кончик каломельного электрода. После первого заметного отклонения стрелки гальванометра записывают еще 4 - 5 показаний прибора и строят кривую. [4]
Исходный титрующий раствор, 1СГ3 М раствор хлорной кислоты. [5]
Рабочий титрующий раствор, 1 ( Г М раствор хлорной кислоты. [6]
Прибавление титрующего раствора В в объеме v разбавляет объем V первоначального раствора. [7]
Подача титрующего раствора при подходе к эквивалентной точке импульсная. [8]
Концентрация титрующего раствора не должна превышать 1 г-экв / л, так как смешение концентрированных растворов кислот и щелочей, кроме теплоты нейтрализации, сопровождается выделением теплоты разбавления. [9]
Прибавление титрующего раствора В в объеме о разбавляет объем V первоначального раствора. [10]
Прибавление титрующего раствора В в объеме v разбавляет объем V первоначального раствора. [11]
Концентрация титрующего раствора не должна превышать 1 г-экв / л, так как смешение концентрированных растворов кислот и щелочей, кроме теплоты нейтрализации, сопровождается выделением теплоты разбавления. [12]
Для простоты титрующий раствор берут сравнительно концентрированным, так что изменением объема в процессе титрования можно пренебречь. [13]
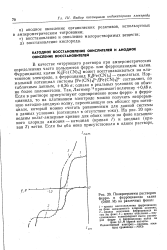 |
Полярограммы растворов. [14] |
В качестве титрующего раствора при амперометрических определениях часто пользуются ферри - или ферроцианидом калия. Феррицианид калия Кз [ Ре ( СЫ) е ] может восстанавливаться на платиновом электроде, а ферроцианид K4 [ Fe ( CN) 6 ] - окисляться. Нормальный потенциал системы [ Fe ( CN) 6 ] 3 - / [ Fe ( CN) 6 ] 4 - составляет, по табличным данным, 0 36 в; однако в реальных условиях он обычно более положителен. Так, Латимер 18 принимает величину 0 48 в. На рис. 20 приведены вольт-амперные кривые для обоих ионов на фоне насыщенного хлорида аммония - катодная ( кривая /) и анодная ( кривая 2) ветви. [15]
Страницы: 1 2 3 4