Флюоритный твердый раствор
Cтраница 1
Флюоритные твердые растворы, богатые ураном, достигнув максимальной степени окисления ( х0 25), не остаются в равновесии с атмосферой при высокой температуре. [1]
Флюоритные твердые растворы окислов металлов IV группы способны поглощать кислород, образуя фазы нестехиометирческого состава ( Me, U) O2 X, в которых избыточный против стехиометрического состава кислород находится в порах кристаллической решетки. [2]
 |
Диаграмма состояния системы UC2 - UO3 - Y2O3. [3] |
Флюоритные твердые растворы этого интервала концентраций устойчивы в атмосфере. [4]
Область однофазного флюоритного твердого раствора в менее окислительных условиях соответственно шире: она существует от 37 до 100 % СеО2; образцы, содержащие менее 37 % СеО2, имеют в своем составе, наряду с флюоритной фазой, закись-окись урана. [5]
 |
Диаграмма состояния системы UC2 - UO3 - Y2O3. [6] |
Богатые ураном флюоритные твердые растворы имеют заполненную кислородную подрешетку и, кроме того, содержат часть избыточного кислорода, внедренного в октаэдрические лоры гранецентрированной решетки. [7]
При меньшем содержании окиси неодима флюоритный твердый раствор сосуществует с закисью-окисью урана, а при составах, содержащих более 65 % NdsO3, переходит в структуру С-типа окислов редких земель - Флюоритному твердому раствору ( см. рис. 5.16, б) соответствует прямая 1, определяющая зависимость параметра решетки твердого раствора от состава. Образцы этих составов дают четкие рентгенограммы с хорошо расщепившимися на си-2 - дублеты линиями. Переход к структуре С-типа наблюдается в составе, содержащем 74 9 % NdOi 5 и дающем завуалированную рентгенограмму с нерасщепленными линиями. [8]
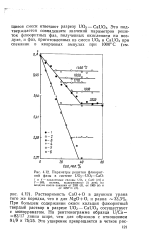 |
Параметры решетки флюорит-ной фазы в системе UOo-UOs-CaO. [9] |
При большем содержании окиси кальция флюоритный твердый раствор в разрезе UCb - CaUO4 сосуществует с моноуранатом. [10]
Как показало тщательное исследование зависимости состава флюоритных твердых растворов, богатых торием, от температуры и давления кислорода, окисленные материалы после достижения равновесного значения х почти не меняют своего состава. Величина х зависит в первую очередь от катионного состава у, а остальные факторы, в том числе температура и давление кислорода, имеют второстепенное значение. Так, значения х, приведенные в табл. 6.4 и полученные Андерсоном и др. [51], в иных условиях ( при 600 С и давлении кислорода 120 атм) совпадают. На рис. 6.6, а показана зависимость параметра решетки флюоритных твердых растворов с разным содержанием двуокиси тория от степени окисления. [11]
Из этих данных можно сделать следующий вывод: флюоритные твердые растворы, полученные в условиях опыта при Г1400 С, по составу близки к растворам, образующимся при высокотемпературном нагреве; отсюда еще раз следует, что заключение Ром-бергера и др. [43] о низкой растворимости двуокиси циркония в двуокиси урана при 1400 - 1500 С сомнительно. [12]
На рис. 5.13 указаны также значения параметров решетки флюоритных твердых растворов 1Ю2 Ж - СеО2, полученных в работе [69] при прокаливании на воздухе при 1200 С соосажденных церий - и уранилнитратов. Сравнение экспериментальных плотностей флюоритных твердых растворов с расчетными также подтверждает это. [13]
 |
Кристаллографические данные ромбоэдрических фаз Rli и Rhll. [14] |
Ромбоэдрические соединения UO3 - 3R203 появляются вследствие структурной перестройки флюоритных твердых растворов, возникающей тогда, когда число вакансий в подрешетке кислорода становится очень большим. [15]
Страницы: 1 2 3