Изученный раствор
Cтраница 3
Для учета влияния электроосмотических потоков было проведено измерение - потенциалов 1 для всех изученных растворов. Для диафрагм использовали порошок из пюттовского стекла, полученный вибропомолом на фарфоровой мельнице. Порошок в дальнейшем обрабатывали хромовой смесью и тщательно промывали сначала в дистиллированной, а затем в бидистиллированнойводе. [31]
Строят на одном графике кривую а - Е для 0 5 М раствора а на другом - зависимости о - Е для всех изученных растворов. [32]
Линейная интерполяция в случае моделирования АХМ, работающих на таких растворах, как вода - аммиак, бромистый литий - вода и других достаточно хорошо изученных растворах, как показали исследования [21, 75 - 78], обеспечивает практически полное совпадение расчетных величин с экспериментальными данными и при этом позволяет производить быструю замену двумерных массивов, соответствующих заданному бинарному раствору. Поэтому при формировании БОТС использованы экспериментальные данные по свойствам, представленные в виде таблиц и тепловых диаграмм. [33]
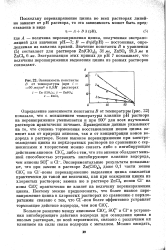 |
Зависимость константы В от температуры ( при i 60 ма / вО 9М растворах. [34] |
Определение зависимости константы В от температуры ( рис. 22) показало, что с повышением температуры влияние рН раствора на перенапряжение уменьшается и при 100 для всех изученных растворов практически исчезает. Приведенные данные указывают на то, что степень торможения восстановления ионов цинка зависит как от природы анионов, так и от концентрации ионов водорода в растворе. Экспериментальные результаты показывают, что при замене в растворе Zn ( C104) 2 даже 0 1 части ионов СЮ 4 на С1 - - - ионы перенапряжение выделения цинка снижается практически до такой же величины, как при осаждении цинка из хлористых растворов; замена же в растворе ZnCl2 ионов СГ на ионы С107 практически не влияет на величину перенапряжения цинка. [35]
 |
Зависимость плотности тока обмена системы Pt Co ( en. i 5 от [ Со ( еп. ] при разных значениях [ Co ( en i ], указанных на. [36] |
Установленное для системы Pt Co ( en) 1 2 ( 0 5 М en, 1 М КС1) совпадение значений а, определенных вблизи равновесного потенциала и при значительных катодных поляризациях, а также равенство единице суммы производных (V.25) и ( V.25), и, следовательно, суммы коэффициентов переноса, свидетельствуют в пользу практического постоянства потенциала % и адсорбционных потенциалов gox и gRea в изученных растворах. Причиной этого, вероятно, является близость формального потенциала системы Со ( en) I2 ( 1 М КС. [37]
Отсюда вытекает и заключение, что растворы, следующие закону Генри - Дальтона, суть односторонне идеальные растворы. Если бы изученные растворы аммиака следовали закону Генри - Дальтона, то мы, разумеется, должны были бы сделать и обратное заключение. Однако факты ясно говорят против этого. [38]
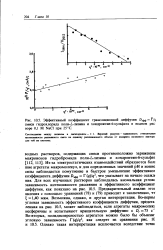 |
Эффективный коэффициент трансляционной диффузии D, Г / q смеси гидрохлорида поли - L-лизина и хондроитин-6 - сульфата в водном рае-воре 0 1 М NaCl при 25 С. [39] |
Из-за электростатических взаимодействий образуются бош шие агрегаты макромолекул, и для определенных значений рН и ионнс силы наблюдается помутнение и быстрое уменьшение эффективно. Для всех изученных растворов наблюдалась аномальная углош зависимость интенсивности рассеяния и эффективного козффициеш диффузии, как показано на рис. 10.5. Предварительный анализ этот явления с помощью уравнений ( 78) и ( 79) приводит к заключению, чт 1 40 мкм. Возможна, однако, и другая интерпретация. [40]
Изучению взаимодействия фосфорорганических соединений с водой посвящено значительное число работ, что объясняется большим практическим и теоретическим интересом к подобным системам. Однако даже в случае сравнительно хорошо изученных растворов трибутилфосфата ( ТБФ) в воде отсутствуют согласованные представления о характере взаимодействия между отдельными компонентами. [41]
В случае водородной связи оказывается возможным наблюдать одновременное сосуществование в растворе разных форм межмолекулярной связи. Рассмотрим их вкратце только для наиболее изученных растворов спиртов и воды в различных растворителях. Чистой жидкости на валентном колебании группы ОН соответствует очень широкая и, по-видимому, сложная по своему строению полоса около 3350 см 1, относящаяся к ассоциированным молекулам. При растворении до малой концентрации в СС14 эта широкая полоса, как было показано выше, заменяется узкой и слабой полосой при 3640 см-1 молекул, не связанных водородным мостом. В 1953 г., в результате исследования растворов воды в различных растворителях [5], мною было высказано предположение, что эта полоса, так же как и полоса 3350 см 1, относится к связанным молекулам воды, находящейся в квазиэмульсионном ( мелкодисперсном) состоянии. То же должно относиться и к - спиртам. Более прямое доказательство этого утверждения было получено в нашей лаборатории Буланиным, исследовавшим поведение полосы воды 2100 см 1 в различных растворителях. Эта полоса получается в результате комбинирования деформационного колебания молекул воды с либрационным межмолекулярным. Она сохраняется в тех же растворителях, что и полоса 3520 см 1 и одновременно с ней исчезает в других. Еще более сложный вид имеет спектр растворов спирта или воды, как было показано Пиментелем [6] в азоте, охлажденном до очень низкой температуры. [42]
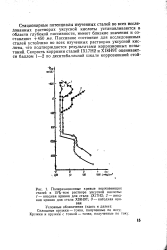 |
Поляризационные кривые нержавеющих сталей в 15 % - ном растворе уксусной кислоты. / - анодная кривая для стали 1Х17Н2. 2 - анодная кривая для стали XI8H9T. 3 - катодная кривая. [43] |
Стационарные потенциалы изученных сталей во всех исследованных растворах уксусной кислоты устанавливаются в области глубокой пассивности, имеют близкие значения и составляют 450 же. Пассивное состояние для исследованных сталей устойчиво во всех изученных растворах уксусной кислоты, что подтверждается результатами коррозионных испытаний. [44]
Можно полагать, что по мере накопления высококачественных термохимических данных для неводных растворов многих электролитов в средах определенного типа различия в величинах разностей A / 7J должны существенно сгладиться. В пользу этого говорит особенно близкое совпадение величин для воды и наиболее подробно изученных растворов в метаноле и формамиде. [45]
Страницы: 1 2 3 4 5