Водный раствор - кислота
Cтраница 1
Водные растворы кислот или оснований имеют соответственно кислую ( рН 7) или щелочную рН 7) реакцию. Практика, однако, показывает, что водные растворы многих солей, а не только кислот и оснований, проявляют щелочную или кислую реакцию - причиной этого является гидролиз солей. [1]
Водные растворы кислот, вследствие их электролитической диссоциации, содержат избыточную концентрацию катионов водорода Н и окрашивают специальные вещества - индикаторы в характерный цвет. Так, лакмус окрашивается в растворе сильной кислоты в красный цвет. Другими словами, красная окраска лакмуса свидетельствует о кислотной среде. [2]
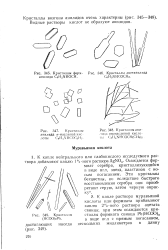 |
Кристаллы форм - [ IMAGE ] Кристаллы ацетанилида анилида C6H5NHOCH. С6Н5КНСОСНз.| Кристаллы анилида - масляной кислоты СеН. зХ НСОСзН -.| Кристаллы ( НСОО аРЬ. [3] |
Водные растворы кислот не образуют анилидов. [4]
Водный раствор кислоты был насыщен мелом, полученный раствор соли подвыпарен на водяной бане и выкристаллизован в эксикаторе над серной кислотой. Соль выделилась в виде пленки, состоящей из мелких кристаллов; в воде растворима очень легко. [5]
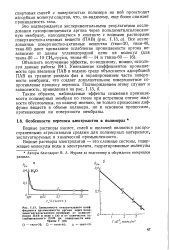
Водные растворы кислоты можно сконцентрировать упариванием в вакууме в вязкую жидкость с концентрацией НВг03 около 50 %, которая хранится без изменений на холоду длительное время. Разбавленные растворы НВг03, не содержащие примесей восстановителей, серной или фосфорной кислоты, вполне устойчивы даже при кипячении. В среде 9 N H2S04 и при кипячении в течение 15 мин. [6]
Водные растворы кислот и оснований имеют, соответственно, кислую ( рН 7) и щелочную ( рН 7) реакцию. Практика, однако, показывает, что не только кислоты и основания, но и соли могут иметь щелочную или кислую реакцию - причиной этого является гидролиз солей. [7]
Водные растворы кислот, солей и щелочей являются распространенными агрессивными средами для полимерных материалов, эксплуатируемых в химической промышленности. [9]
Водные растворы кислоты довольно стойки на свету, но разлагаются при нагревании выше 40 С. При - 20 С растворы НСЮ3 различных концентраций загустевают, но не закристаллизовываются, Крепкий раствор кислоты имеет желтоватый цвет, разбавленный - бесцветный. Разбавленная кислота на холоду запаха не имеет. [10]
Водные растворы кислот, оснований и солей - наиболее широко применяемый и наиболее изученный класс ионных проводников. Хотя в последнее время возросла роль и других видов ионных проводников, водные растворы по-прежнему занимают господствующее положение. Значение водных растворов выходит далеко за пределы собственно электрохимии; они встречаются практически во всех сферах деятельности человека. Исключительна роль водных растворов ( внутриклеточной жидкости) в биологических и физиологических процессах в живой природе. [11]
Водный раствор кислоты, нейтрализованный аммиаком, дает с раствором хлористого кальция белый нерастворимый в уксусной и растворимый в соляной кислоте осадок. [12]
Водный раствор кислоты ( 1: 10), пересыщенный аммиаком, не должен реагировать с раствором щавелевокислого аммония. [13]
Водный раствор кислоты ( 1: 5) не должен изменяться от прибавления разведенной серной кислоты или сероводородной воды. [14]
Водные растворы кислот изменяют окраску индикаторов и являются электролитами. [15]
Страницы: 1 2 3 4