Водный раствор - неэлектролит
Cтраница 3
Ниже приведены данные о коэффициентах bv для водных растворов неэлектролитов различной природы. [31]
 |
Зависимость, в реакции от длины ал-квльной группы при 298 К. [32] |
Приведенные результаты демонстрируют несомненное наличие связи между строением водных растворов неэлектролитов и характеристиками ( равновесными и кинетическими) реакций, протекающих в этих растворах. Обсуждение по необходимости остается пока, главным образом, качественным как в силу отсутствия количественной теории самих водных растворов, так и ввиду невозможности надежной оценки состава сольватных оболочек. [33]
Перед тем, как приступить к обсуждению избыточной теплоемкости водных растворов неэлектролитов, необходимо коснуться вопроса о точности определения значений Ср. Поскольку величина Ср составляет лишь небольшую долю от общей теплоемкости раст вора ( нередко не более 1 - 2 %), то оценка погрешности вычисли емых по соотношению (V.4) значений Ср совершенно необходима. [34]
Формулой ( 9) пользуются для вычисления осмотического давления водных растворов неэлектролитов при 0 С по данным криоско-пического метода. [35]
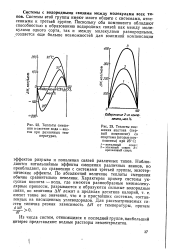 |
Теплоты смешения в системе вода - ацетон при различных температурах.| Теплоты смешения ацетона ( первый компонент со спиртами ( вторые компоненты при 25 С. [36] |
Из числа систем, относящихся к последней группе, наибольший интерес представляют водные растворы неэлектролитов. [37]
В литературе имеется лишь небольшое число данных об избыточной энергии Гиббса GE водных растворов неэлектролитов. Поэтому не представляется возможным сделать обстоятельный анализ зависимости GE ( x) для разных классов растворов. Мы рассмотрим только данные о GE ( x) для водных растворов спиртов, циклических эфиров и некоторых других неэлектролитов. Кроме того, нам хотелось бы коснуться одного общего вопроса, а именно: обсудить черты сходства и различия избыточных термодинамических функций GE, HE и TSE. [38]
На рис. V.14 приведены наиболее характерные диаграммы ХБ ( х) для водных растворов неэлектролитов. [39]
Довольно часто используют также еще одни метод применения теории ММ к анализу водных растворов неэлектролитов. В нем просто рассматривают коэффициенты разложений избыточных термодинамических функций разбавленного раствора, полученные путем математической обработки экспериментальных данных. Сопоставление величин и знаков этих коэффициентов для неэлектролитов различной природы позволяет получить некоторую информацию о межмолекулярных взаимодействиях. [40]
На рис. 3.12 представлены зависимости XQTJQ для растворов KF и КС1 в водных растворах неэлектролитов. Из рисунка следует, что несмотря на примерно равные подвижности ионов К, F - и С1 - поведение этих солей совершенно различное в разных по своей природе смесях растворителей, и постоянство A QTJ о для них не сохраняется. [41]
Существует обзор, сделанный Наберухиным и Роговым [ 13в ], по структурам водных растворов неэлектролитов. [42]
Этот факт кажется на первый взгляд удивительным, так как исследования термодинамических свойств водных растворов неэлектролитов несомненно имеют важное научное и практическое значение. Однако не следует забывать, что энтальпии смешения, как правило, исследуют в системах с полной взаимной растворимостью компонентов. Поскольку число жидких неэлектро - литов, обладающих при обычных условиях свойствами полной смешиваемости с водой весьма ограничено, то и число возможных объектов для изучения НЕ ( х) во всем концентрационном интервале также невелико. [43]
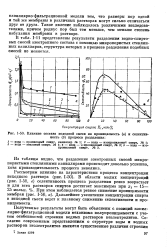 |
Влияние состава исходной смеси на проницаемость ( а и селективность ( б процесса разделения. [44] |
Полученные результаты могут быть объяснены с позиций капиллярно-фильтрационной модели механизма полупроницаемости с учетом особенностей строения водных растворов неэлектролитов. [45]
Страницы: 1 2 3 4