Водный раствор - бикарбонат - натрий
Cтраница 1
Водный раствор бикарбоната натрия имеет слабо выраженный щелочной характер, поэтому на животные и растительные ткани он не действует. Растворимость бикарбоната натрия в воде невелика. С повышением температуры она несколько увеличивается. В табл. 26 приведены данные о растворимости NaHCO3 в воде при различных температурах. [1]
Водный раствор бикарбоната натрия имеет слабо выраженный щелочной характер, поэтому на животные и растительные ткани он не действует. Растворимость бикарбоната натрия в воде невелика. С повышением температуры она несколько увеличивается. В табл. 34 приведены данные о растворимости NaHCO3 в воде при различных температурах. [2]
Водный раствор бикарбоната натрия имеет нейтральную реакцию. Он используется в медицине ( назначается при повышенной кислотности желудка) и в пищевой промышленности. [3]
В водном растворе бикарбоната натрия р р - дихлордиэтилсуль-фид реагирует с аминогруппами таких аминокислот как глицин аланин, лииин. В щелочной среде иприт реагирует с карбоксильными группами. [4]
 |
Схема включения ячеек электролитического выпрямителя. [5] |
Если в водный раствор бикарбоната натрия погрузить свинцовый и алюминиевый электроды и присоединить их к источнику переменного тока с напряжением 60 - 100 в, то в цепи будет наблюдаться пульсирующий ток одного направления. [6]
Корпус огнетушителя заполнен водным раствором бикарбоната натрия с добавкой поверхностно-активного вещества - солодкового экстракта. Отдельно в полиэтиленовом стакане содержится кислотная часть заряда - смесь сульфата железа ( III)) с серной кислотой. При этом кислотная и щелочная части заряда перемешиваются и за счет выделения диоксида углерода образуется пена, которая сильной струей выбрасывается через спрыск. Огнетушитель ОХП-10 образует примерно 90 л пены. Попадая на горящий объект, пена изолирует его от кислорода воздуха и резко уменьшает испарение горящей жидкости, что приводит к прекращению горения. Огнетушащий эффект пены связан также с ее охлаждающим действием. [7]
Кислота растворена в водном растворе бикарбоната натрия. [8]
При рН 7 4 ( водный раствор бикарбоната натрия) время 50 % гидролиза GB при добавлении 0 1 % перекиси водорода сокращается с 8 ч до 84 мин, а при рН 8 4 ( водный раствор фосфата натрия) - с 84 мин до 12 мин. Для дегазации GB и других фтора нгид ридов алкилфосфоновых кислот рекомендуются 3 % растворы перекиси водорода в щелочах; в них разложение ОВ происходит примерно в 50 раз быстрее, чем при щелочном гидролизе. [9]
При рН 7 4 ( водный раствор бикарбоната натрия) время 50 % гидролиза GB при добавлении 0 1 % перекиси водорода сокращается с 8 ч до 84 мин, а при рН - 8 4 ( водный раствор фосфата натрия) - с 84 мин до 12 мин. Для дегазации GB и других фтора гидридов алкнлфосфоиовых кислот рекомендуются 3 % растворы перекиси водорода в щелочах; в них разложение ОВ происходит примерно в 50 раз быстрее, чем при щелочном гидролизе. [10]
После обработки кислоты стехиометрическим количеством водного раствора бикарбоната натрия, нагревания до растворения и выпаривания досуха получают натриевую соль. [11]
Обработка названных солей водой или водным раствором бикарбоната натрия приводит к соответствующим О-ацети-лированным сахарам, содержащим свободную аминогруппу. При строгом контроле условий реакции гликозидная связь не затрагивается. [12]
Анилин под действием иода в присутствии водного раствора бикарбоната натрия дает n - иоданилин. Обычным препаративным методом получения хлортолуолов и бромтолуолов является реакция Занд-мейера. [13]
В результате обработки хлороформного раствора III водным раствором бикарбоната натрия образуется соответствующее им. [14]
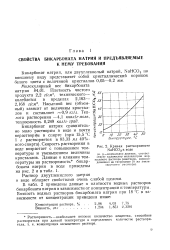 |
Кривая растворимости NaHCO3 в воде. [15] |
Страницы: 1 2 3