Водный раствор - пероксид - водород
Cтраница 1
Водные растворы пероксида водорода широко используются для отбелки различных материалов, для обеззараживания сточных вод. Пероксид водорода применяют как окислитель ракетного топлива. [1]
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки. [2]
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированТГых растворах пероксида водорода содержатся стабилизирующие добавки. [3]
Водные растворы пероксида водорода более устойчивы: и прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированных растворак пероксида водорода содержатся стабилизирующие добавки. [4]
Водные растворы пероксида водорода более устойчивы: в прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки. [5]
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. Пергидроль - раствор, который поступает в продажу, - содержит 30 % HzOz. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки. [6]
Водные растворы пероксида водорода широко используются для отбелки различных материалов, для обеззараживания сточных вод. Пероксид водорода применяют как окислитель ракетного топлива. [7]
Водные растворы пероксида водорода широко используются для отбелк. Пероксид водорода применяют как окислитель ракетного топлива. [8]
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки. [9]
Водные растворы пероксида водорода широко используют для отбелки различных материалов. Пероксид водорода применяют как окислитель ракетного топлива. [10]
Водные растворы пероксида водорода более устойчивы; в прохладном месте они могут сохраняться довольно долго. В нем, а также в высококонцентрированных растворах пероксида водорода содержатся стабилизирующие добавки. [11]
Когда водный раствор пероксида водорода реагирует с образованием газообразного кислорода и жидкой воды, происходит заметное выделение тепла. Количество выделяемой теплоты в некоторой степени зависит от температуры, при которой проводится реакция, однако при 25 С-именно такую температуру называют комнатной температурой при измерениях и табулировании теплот реакций-при разложении 1 моля Н2О2 выделяется 94 7 кДж тепла. [12]
Через водный раствор пероксида водорода пропускают хлор. [13]
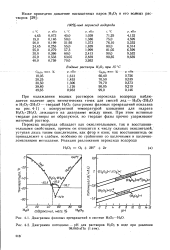 |
Диаграмма фазовых превращений в системе НгСЬ - Н2О.| Диаграмма потенциал - рН для растворов Н2О2 в воде при давлении. [14] |
При охлаждении водных растворов пероксида водорода наблюдается наличие двух эвтектических точек для смесей лед - г - НзСЬ НгО и Н2О2 - 2Н2О - твердый НзОг ( диаграмма фазовых превращений показана на рис. 4 - 1) с конгруэнтной температурой плавления для гидрата НгО2 - 2Н2О, лежащего на диаграмме между ними. При этом истинные твердые растворы не образуются, но твердые фазы прочно удерживают маточный раствор. [15]
Страницы: 1 2 3