Растворение - сурьма
Cтраница 1
Растворение сурьмы и висмута наблюдается в интервале ( - 0 35) - ( - 0 10) в. Концентрацию ионов металлов находят методом добавок. [1]
Растворение сурьмы для определения примесей Са, А1, Сг и Si производят следующим образом. Навеску измельченной и промытой сурьмы обрабатывают концентрированной HNO3 на электроплитке, покрытой слоем асбеста. После превращения сурьмы в сурьмяную кислоту выпаривают НМО3 досуха и слегка прокаливают на плитке. Затем приливают концентрированную НВг, смачивая стенки чашки или тигля, и выпаривают досуха. Повторяют выпаривание с НВг еще 2 - 3 раза. Неудаленные незначительные количества сурьмы ( 25 - 100 мкг) либо не мешают дальнейшему анализу, либо могут быть замаскированы. [2]
Растворение сурьмы для определения примесей Са, А1, Сг и Si производят следующим образом. Навеску измельченной и промытой сурьмы обрабатывают концентрированной HNO3 на электроплитке, покрытой слоем асбеста. После превращения сурьмы в сурьмяную кислоту выпаривают HNO3 досуха и слегка прокаливают на плитке. Затем приливают концентрированную НВг, смачивая стенки чашки или тигля, и выпаривают досуха. Повторяют выпаривание с НВг еще 2 - 3 раза. Неудаленные незначительные количества сурьмы ( 25 - 100 мкг) либо не мешают дальнейшему анализу, либо могут быть замаскированы. [3]
Величину тока растворения сурьмы измеряют графически по перпендикуляру, опущенному из вершины зубца до продолжения отрицательной ветви кривой. [4]
Величину тока растворения сурьмы измеряют графически по перпендикуляру, опущенному из вершины зубца до продолжения отрицательной ветои кривой. [5]
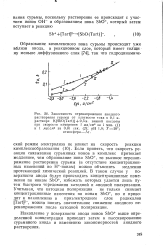
Сильное влияние на растворение сурьмы в пассивной области оказывает гидродинамический режим электролиза и концентрация тартрат-ионов, в противоположность растворению в активной области. [7]
Для проверки полноты растворения сурьмы фольгу опускают в 5 % - ный раствор соляной кислоты; если при этом на фольге остаются темные пятна сурьмы, то обработку перекисью натрия повторяют. [8]
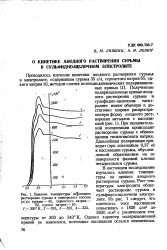 |
Влияние температуры на анодное растворение сурьмы в электролите состава ( г / л. сурьмы - 35, сернистого натрия. [9] |
При незначительной поляризации происходит растворение сурьмы с образованием тиоантимоната натрия. Дальнейшая поляризация приводит ( при потенциале 0 37 в) - к пассивации сурьмы, обусловленной образованием на ее поверхности фазовой пленки четырехокиси сурьмы. [10]
По окончании выделения спираль для растворения сурьмы погружают в узкий стаканчик с водой, прибавляют 1 г Na2O2 и кипятят около 10 мин. Раствор выпаривают с H2SO4 и колориметрируют по вышеуказанному. [11]
Приведенные результаты показывают, что растворение сурьмы на участке / поляризационной кривой происходит, по всей вероятности, с непосредственным участием гидрок-сил-ионов или воды и что процесс сопровождается концентрационной поляризацией по Н - ионам. [12]
Эти результаты свидетельствуют о том, что пассивация и растворение сурьмы в пассивной области определяются диффузионными ограничениями по тартрат-ионам. [13]
Медь и висмут не растворяются и остаются в шламе, тем не менее, вследствие близости их равновесных потенциалов потенциалу растворения сурьмы, при большой анодной поляризации они частично ионизируются. Попав в электролит, эти примеси осаждаются на катоде. Золото и серебро практически целиком остаются в шламе. [14]
Страницы: 1 2 3