Растворение - фенол
Cтраница 1
Растворение фенола в воде Реактивы и материалы: фенол жидкий. [1]
Для растворения фенола и связывания образующейся иодис-товодородной кислоты процесс ведут в щелочной среде. Избыток иода титруют тиосульфатом после подкисления. [2]
Теплоты растворения фенола в бензоле и пиридине соответственно равны 2530 и - 630 кал / моль [ В. [3]
Теплота растворения фенола в бензоле и пиридине соответственно равна 2530 и - 630 кал / моль. О чем свидетельствуют эти результаты, если теплота плавления фенола равна 2730 кал / моль. [4]
Теплоты растворения фенола в бензоле и в пиридине соответственно равны 2530 и - 630 кал / моль [ В. [5]
Теплоты растворения фенола в бензоле и в пиридине соответственно равны 2530 и - 630 кал молъ [ В. [6]
Кислоту приготовляют растворением фенола в серной кислоте. [7]
Образующийся при растворении фенола в щелочи фен-окси-анион более активный нуклеофильныи реагент, чем фенол. Ацилирование фенолов хлор ангидридами в щелочной среде осуществляется по методу Шоттен-Баума - на: к водно-щелочному раствору фенола добавляют при встряхивании хлорангидрид кислоты. Таким способом получают фенилбензоат, бензонафтол и другие соединения. Аналогично получают сложные эфиры фенолов в щелочной среде путем ацилирования их ангидридами кислот, например, р-нафтилацетат. [8]
При этом происходило растворение фенола в воде и выделение растворенной в нем смолы. [9]
Смесь нагревалась и после растворения фенола взбалтывалась в течение 20 мин. Навеска смеси примерно 100 г помещалась в круглодонную колбу, и фенол отгонялся паром по вышеописанной методике. [10]
Это объясняется не только растворением фенолов в хинолине, но и химическим взаимодействием. Известно применение в качестве экстрагентов каменноугольных и других масел. Однако применение масел затрудняется их склонностью образовывать с водой и щелочью стойкие эмульсии. [11]
Синтез альдегидов по Гаттерману осуществляется растворением фенола для его простого эфира в бензоле или эфире, обработкой раствора цианистым водородом и затем прибавлением хлористого алюминия при обычной температуре или лучик1 на холоду. [12]
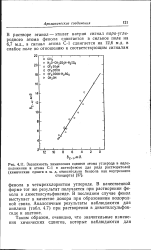 |
Зависимость химических сдвигов атома углерода в пара-положении и атома С-1 в аиетофеноне для ряда растворителей ( химические сдвиги в м. д. относительно бензола как внутреннего стандарта. [13] |
В качественной форме тот же результат получается при растворении фенола в диметилсульфоксиде. В последнем случае фенол выступает в качестве донора при образовании водородной связи. Аналогичные результаты наблюдаются для анилина ( табл. 4.7) при растворении в диметилсульфоксиде и ацетоне. [14]
В пробирку с 1 - 1 5 г фенола прибавляют несколько капель воды до растворения фенола и образования однородной жидкости. В другой пробирке смешивают 2 мл концентрированной азотной кислоты ( 1 4) с 2 5 мл воды. Полученную разбавленную азотную кислоту медленно приливают каплями ( при встряхивании и охлаждении) к смеси фенола и воды, поддерживая температуру 20 - 25 С. Через 15 мин образовавшуюся темную жидкость выливают в 15 мл воды. После отстаивания смеси воду сливают, а выделившуюся полужидкую массу еще раз промывают 15 мл воды, затем масло переливают в большую пробирку, добавляют 5 - 7 мл воды, опускают кусочки пористого кирпича в качестве кипятильника и закрывают ее пробкой со вставленной отводной нисходящей трубкой. Пробирку укрепляют наклонно в лапке штатива. Конец отводной трубки погружают в охлаждаемый приемник-пробирку. Перегонку следует вести до тех пор, пока перегоняющаяся жидкость при охлаждении будет выделять желтые кристаллы. [15]
Страницы: 1 2 3 4