Растворение - германий
Cтраница 4
Из рис. 33 видно, что при введении в раствор КзРе ( С1) 6 ток, текущий через фазовую границу, больше максимально возможного дырочного тока в полупроводнике и что предельный анодный ток реакции растворения германия увеличивается так же, как и при действии света или при повышении температуры. [46]
Металлический германий легко растворяется в царской водке, в растворах гипохлоритов или гидроокисей щелочных металлов ( в присутствии перекиси водорода) и в расплавах щелочей, перекисей, нитратов и карбонатов щелочных металлов. В результате растворения германия в расплавах NaOH, КОН, Na202, K202, KN03 или К2С03 образуются растворимые соли германия. [47]
Картина последующих процессов такова: узкая струя тока ( плотностью порядка 105 а / см2 и сечением порядка 10 - 5 см2) выделяет на границе жидкий индий-германий тепло Пельтье. Это способствует растворению германия в жидкой фазе индия. В связи с этим фронт жидкой фазы продвигается по трубке тока эмиттерной струи через рекристаллизованный слой эмиттера и область базы к коллектору. [48]
Иначе обстоит дело при анодном растворении германия в щелочных растворах. В этом случае на скорость растворения германия наряду с его электрофизическими свойствами большое влияние оказывает концентрация гидроксильных ионов. [49]
Скорость разложения перекиси водорода проходит через максимум с увеличением концентрации щелочи. Интересно, что максимальная скорость растворения германия наблюдается при той же приблизительно концентрации щелочи, что и максимальная скорость разложения перекиси водорода до опыта при данной температуре. [50]
 |
Создание р - п-перехода методом вплавления. [51] |
При нагревании до 500 С происходит растворение германия в расплавленном индии, а при последующем медленном охлаждении - кристаллизация германия с примесью индия. Поскольку германий с примесью индия имеет проводимость р-типа, то между ним и основным кристаллом образуется р - л-переход. [52]
При определении металлического германия фильтр помешают в химический стакан, смачивают спиртом и обрабатывают 10 мл раствора NaOH и 0 5 мл пергидроля. Стакан с содержимым нагревают на плитке до растворения германия и переливают раствор в коническую колбу. Фильтр повторно обрабатывают 5 мл раствора щелочи при нагревании, отжимают и раствор сливают в ту же колбу. Колбу закрывают воронкой и при медленном кипении раствора в течение 15 мин разрушают перекись водорода. Раствор охлаждают и нейтрализуют соляной кислотой ( d 1 19) до нейтральной реакции по лакмусу. [53]
Фильтр помещают в стакан, смачивают этиловым спиртом ( если фильтр перхлорвиниловый) и обрабатывают 10 мл 1 % раствора едкого натра и 0 5 мл пергидроля. Стакан с содержимым нагревают на плитке до растворения германия и переливают раствор в коническую колбу. Фильтр вновь обрабатывают 5 мл щелочи при нагревании, сливают жидкость в ту же колбу и отжимают фильтр стеклянной палочкой. Колбу закрывают воронкой для фильтрования и кипятят в течение 15 минут для разрушения перекиси водорода при слабом нагревании. По мере выкипания раствора добавляют 3 - 4 мл дистиллированной воды. Раствор охлаждают и нейтрализуют концентрированной соляной кислотой до нейтральной реакции по лакмусовой бумаге. Если проба содержит только двуокись германия, фильтр обрабатывают раствором едкого натра без пергидроля и сразу нейтрализуют. [54]
При определении металлического германия фильтр помещают в химический стакан, смачивают спиртом п обрабатывают 10 мл раствора NaOH и 0 5 мл пергидроля. Стакан с содержимым нагревают на плитке до растворения германия и переливают раствор в коническую колбу. Фильтр повторно обрабатывают 5 мл раствора щелочи при нагревании, отжимают и раствор сливают в ту же колбу. Колбу закрывают воронкой и при медленном кипении раствора в течение 15 мин разрушают перекись водорода. [55]
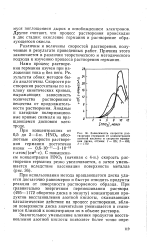 |
Зависимость скорости растворения германия от концентрации азотной кислоты и скорости вращения диска, об / мин. / - 125. 2 - 495. 3 - И72. [56] |
Различны и величины скоростей растворения, полученные в результате проведенных работ. Причина этого заключается в различии теоретического и методического подхода к изучению процесса растворения германия. [57]
Единый цикл вплавления и присоединения выводов к электродам сокращает затраты времени по сравнению с раздельными операциями, но налагает определенные ограничения. Так, толщина позолоты на кристал-лодержателе должна находиться в весьма узких пределах во избежание чрезмерного растворения германия и, как следствие этого, уменьшения толщины пластинки в зоне базового контакта. Ряд конструктивных требований, предъявляемых к кассетам для сплавления, затрудняет контроль размеров и соосности электродов. [58]
Розанова и Катаев [251] и Геришер и Миндт [252], сделали такой вывод для реакции растворения германия в кислых растворах, содержащих перекись водорода. В работе Геришера и Воллем-Матеса [253] предполагается химическое растворение арсенида галлия Ga-As в растворах с перекисью водорода и с бромом. Пенов, Косаковская, Ботнева, Андреева и Жук [256] на основе экспериментальных результатов считают, что химическому растворению подвергается не только железо, но и никель. Шваб и Зосимович [257] обнаружили, что при электроосаждении марганца наряду с его выделением происходит и растворение металла со скоростью, не зависящей от потенциала. Авторы [257] предположили, что растворение марганца происходит по химическому механизму. Ловден [258] предложил теорию для объяснения найденного им избыточного растворения алюминия в кислых растворах электролитов при анодной поляризации, основанную на представлении о химическом механизме этого процесса. Им был сделан и подтвержден вывод, что с ростом анодного тока вклад химической реакции в этот процесс снижается. По данным Цветновой и Красилыцикова [259], по химическому механизму может растворяться титан в серной кислоте. Гильберт [260] при исследовании электроосаждения железа на золотом катоде из сульфатных растворов солей железа обнаружил аномалии, позволившие принять, что при очень отрицательных потенциалах ионы железа разряжаются по туннельному механизму до изолированных атомов, которые, в свою очередь, растворяются, причем анодный ток на процесс растворения не затрачивается. Беркович [ 260а ], а также Махбуба и Иофа [261] подтвердили вывод о возможности растворения железа по химическому механизму. [59]
С уменьшением температуры оба максимума сдвигаются в сторону больших концентраций щелочи. Как показали дальнейшие исследования, скорость разложения перекиси водорода оказывает лишь косвенное влияние на скорость растворения германия, изменяя концентрацию свободной перекиси водорода в растворе. [60]
Страницы: 1 2 3 4 5