Растворимость - кислота
Cтраница 1
Растворимость кислоты в растворе щелочи зависит от двух факторов - ионизационного равновесия, количественным выражением которого является константа ионизации, и растворимости нейтральной формы вещества. Так, энантовая кислота легко растворяется в буферном растворе с рН 7, в то время как другой член гомологического ряда - стеариновая кислота - практически нерастворима в таком растворе, хотя величины рКа этих кислот одинаковы. Причина этого - крайне малая растворимость недиссоциированной стеариновой кислоты. [1]
Растворимость кислоты при комнатной температуре составляет примерно 4 г на 100 мл. [2]
Вследствие растворимости фенилсульфонилфторуксусной кислоты в воде эфирный экстракт после извлечения кислоты не промывают водой. [3]
Изучение растворимости грег-бутиладипиновой кислоты ( ТБАК) в азотной кислоте в зависимости от температуры показало, что для уменьшения потерь ее с фильтратом и промывными водами необходимо про - - водить кристаллизацию при температуре 0 - 5 С. [4]
Температура плавления и растворимость кислот уменьшаются в гомологическом ряду с РОСТОЕЛ молекулярного веса. [5]
 |
Технологическая схема производства диметилтерефталата. [6] |
Это позволяет повысить растворимость кислот в реакционной массе, сократить число стадий и аппаратов и проводить разделение продуктов только после этерификации. [7]
Используя возможность снижения растворимости кислот применением насыщенного раствора солей в качестве водной фазы, кислоты удается сополимеризовать непосредственно друг с другом, и необходимость в омылении получаемых продуктов отпадает. [8]
Условия анализа определяются растворимостью кислоты. [9]
Известно также, что растворимость алотной кислоты в органической фазе возрастает с увеличением концентраций образующихся нитросоединений. Наконец, надежно установлено, что ароматические углеводороды нитруются, в гомогенных водных растворах, но механизм реакции может быть иным, чем в органических растворах. Принимая это во внимание, ясно, что в двухфазной системе реакция может протекать одновременно в обеих фазах, хотя и с не одинаковой скоростью. Во всяком случае скорость зависит от положения и глубины реакционной зоны. Тогда возникает основной вопрос: можно ли считать реакцию гомогенной в каждой фазе. Это представляется маловероятным, если иметь в виду, что подобные реакции исключительно быстры и могут протекать со взрывом. [10]
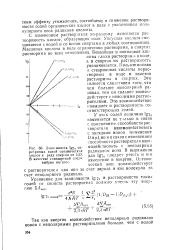 |
Зависимость lg - ( 0 серебряных солей органических кислот в ряду спиртов от I / O. В качестве стандартной среды выбран метанол. [11] |
С изменением растворителя по-разному изменяется растворимость кислот, образующих соли. Уксусная кислота смешивается с водой и со всеми спиртами в любых соотношениях. Масляная кислота в воде ограниченно растворима, в спиртах растворима во всех отношениях. Бензойная и нониловая кислоты плохо растворимы вводе, а в спиртах их растворимость увеличивается. Пальмитиновая и стеариновая кислоты нерастворимы в воде и заметно растворимы в спиртах. Это является следствием того, что чем больше неполярный радикал, тем он сильнее взаимодействует с невоаными растворителями. Это взаимодействие повышает и растворимость соответствующих солей. [12]
По мере увеличения молекулярного веса растворимость кислот в воде уменьшается. Высшие карбоновые кислоты в воде не растворяются и являются твердыми нелетучими веществами без запаха. Все карбоновые кислоты хорошо растворяются в спирте и эфире. [13]
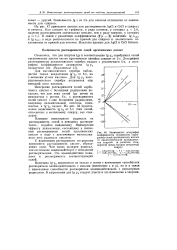 |
Зависимость логарифма коэффициента активности серебряных солей органических кислот от диэлектрической проницаемости спиртов ( в качестве стандартной среды выбран метиловый спирт. [14] |
С изменением растворителя по-разному изменяется растворимость кислот, образующих соли. Чем менее полярен радикал, тем он сильнее взаимодействует с неводными растворителями. Это взаимодействие повышает и растворимость соответствующих солей. [15]
Страницы: 1 2 3 4