Растворимость - комплекс
Cтраница 2
При попытке авторов определить растворимость основных хроматных комплексов было обнаружено, что комплексы не растворяются IB воде, как целое, и что вода является фактором, вызывающим изменение их состава. [16]
При попытке авторов определить растворимость основных хроматных комплексов было Обнаружено, что комплексы не растворяются IB воде, как целое, и что вода является фактором, вызывающим изменение ж состава. [17]
При попытке авторов определить растворимость основных хромагных комплексов было - обнаружено, что комплексы не растворяются в иоде, как целое, и что вода является фактором, вызывающим изменение их состава. [18]
Различия в комплексообразующей способности или растворимости комплексов используют довольно часто. На первом эффекте основано большинство методов комплексометрического титрования. Примером использования различий в растворимости является титрование по Фольгарду, при котором Ag и роданид калия в азотнокислой среде дают желтый нерастворимый роданид серебра. [19]
Несомненно, важную роль в растворимости комплексов играет энергия кристаллической решетки. При прочих равных условиях с увеличением энергии кристаллической решетки растворимость должна уменьшаться. Известно, что комплексы типа зеленой соли Магнуса очень мало растворимы. Их кристаллическая решетка имеет колоночное строение с чередованием плоскостей катиона и аниона. В соли Магнуса [ Pt ( NH3) 4 ] [ PtClJ расстояние платина-платина равно 0 323 нм. Столь малое расстояние означает, что имеет место взаимодействие между атомами платины с образованием химической связи. Образование химической связи платина-платина приводит к увеличению энергии кристаллической решетки. [20]
При попытке авторов, определить растворимость основных хроматных комплексов было обнаружено, что комплексы не растворяются в воде, как целое, и что вода является фактором, вызывающим изменение ик состава. [21]
Вероятно, это связано с улучшением растворимости комплексов в нафтеновой среде. [22]
Однако в связи с тем, что растворимость комплекса тория с ТТЛ в бензоле весьма мала, этот метод используется в основном для экстракции малых количеств тория. [23]
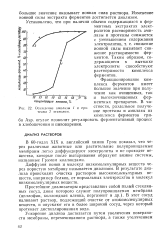 |
Осаждение амилазы / и про. [24] |
Таким образом, содержащиеся в вытяжке электролиты способствуют растворимости комплекса ферментов. [25]
Олово количественно экстрагируется в виде комплекса с NaDDC ( растворимость комплекса 0 1 г / 100 мл) при рН 4 - 6 2 четыреххлористым углеродом; в более щелочной области ( при рН 7 5) этот элемент практически не извлекается даже в присутствии 0 01 - 0 03 М растворов реагента. [26]
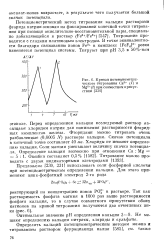 |
Криваяпотенциометри-ческого титрования Са2 ( 1 и Mg2 ( 2 при совместном присутствии. [27] |
Перед определением кальция исследуемый раствор насыщают хлоридом натрия для понижения растворимости фторид-ных комплексов железа. Фторидами можно титровать очень разбавленные ( 0 0005 N) растворы кальция. Скачок потенциала в конечной точке составляет 40 мв. Хлориды не мешают определению кальция. Соли магния уменьшают величину скачка потенциала. [28]
Однако Кузнецов и Большакова [5] отметили неблагоприятное влияние карбоксильной группы на растворимость комплекса родамина и предложили использовать бутиловый эфир н-бутил), называемый бутилродамином. [29]
В общем случае глубина обесцвечивания определяется степенью диссоциации карбоксильных групп и растворимостью гидроксидных комплексов, а оптимум значений рН ( рис. VI.8) - соотношением между числом диссоциированных карбоксильных групп и количеством малорастворимых продуктов гидролиза коагулянта. Некоторое несоответствие значений экспериментально найденных оптимальных рН и рассчитанных с помощью уравнения (VI.6) может быть объяснено или неравновесным состоянием системы, или погрешностями расчета, связанными с недоучетом влияния других параметров. [30]
Страницы: 1 2 3 4