Растворимость - кристаллогидрат
Cтраница 3
Если нанести на диаграмму, подобную изображенной на рис. 3.1, точку G состава кристаллогидрата при температуре его плавления ( рис. 3.3) и опустить из этой точки перпендикуляр на ось абсцисс, то этот перпендикуляр GF разделит диаграмму на две части, аналогичные диаграмме на рис. 3.1. Линия НА по-прежнему является линией насыщения льдом, AGE - кривая растворимости кристаллогидрата состава F, и поэтому области AGR и GQE есть поля кристаллизации кристаллогидрата. В точке А кристаллизуется эвтектическая смесь льда и кристаллогидрата, а в точке Е - эвтектическая смесь кристаллогидрата F и безводной соли S. [31]
Примером может служить кривая растворимости сульфата натрия. Растворимость кристаллогидрата сульфата натрия Na2SO4 - 10H2O возрастает с повышением температуры от 0 до 32 28 С. Выше 32 28 С эта соль теряет воду. Безводный сернокислый натрий при повышении температуры снижает свою растворимость. [32]
Растворимость сульфата кальция как в чистой фосфорной кислоте, так и в смесях ее со свободной серной кислотой, а также з растворах монокальцийфосфата в фосфорной кислоте хорошо изучена. На рис. IX-19 приведена растворимость кристаллогидратов сульфатов кальция в растворах фосфорной кислоты при 80 С. Ангидрит является стабильной фазой при всех концентрациях фосфорной кислоты, поскольку он обладает наименьшей растворимостью. [33]
Области существования этих кристаллогидратов находятся в пределах заштрихованных криволинейных треугольников: в треугольнике S M - тетрагидрат, в треугольнике S MMi - тригидрат, в треугольнике S2NM - дигидрат. Эти области ограничены кривой N M MN растворимости кристаллогидратов в кислых растворах и линиями перехода кристаллогидратов. Ниже и левее линии растворимости находится область ненасыщенных кислых растворов. [34]
Бромистый натрий принадлежит к типу солей, образующих с водой кристаллогидраты; он дает соединения с двумя и пятью молекулами воды. Поэтому кривая растворимости бромистого натрия состоит из нескольких ветвей растворимости соответствующих кристаллогидратов, пересекающихся в точках превращения. [35]
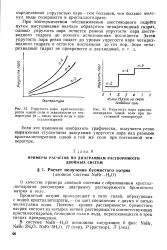 |
Упругость пара кристаллогидратов одной соли в зависимости от температуры ( п - число молей воды в кристаллогидрате.| Упругость пара кристаллогидратов одной соли при постоянной температуре. [36] |
Бромистый натрий принадлежит к типу солей, образующих с водой кристаллогидраты, - он дает соединения с двумя и пятью молекулами воды. Поэтому кривая растворимости бромистого натрия состоит из четырех ветвей растворимости соответствующих кристаллогидратов, безводной соли и льда, пересекающихся в трех точках превращения. [37]
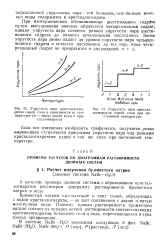 |
Упругость пара кристаллогидратов одной соли в зависимости от температуры ( п - число молей воды в кристаллогидрате.| Упругость пара кристаллогидратов одной соли при постоянной температуре. [38] |
Бромистый натрий принадлежит к типу солей, образующих с водой кристаллогидраты, - - он дает соединения с двумя и пятью молекулами воды. Поэтому кривая растворимости бромистого натрия состоит из четырех ветвей растворимости соответствующих кристаллогидратов, безводной соли и льда, пересекающихся в трех точках превращения. [39]
Бромистый натрий принадлежит к типу солей, образующих с водой кристаллогидраты; он дает соединения с двумя и пятью молекулами воды. Поэтому кривая растворимости бромистого натрия состоит из нескольких ветвей растворимости соответствующих кристаллогидратов, пересекающихся в точках превращения. [40]
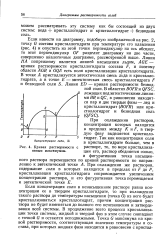 |
Кривая растворимости явным максимумам. [41] |
Если нанести на диаграмму, подобную изображенной на рис. 2, точку G состава кристаллогидрата при температуре его плавления ( рис. 4) и опустить из этой точки перпендикуляр на ось абсцисс, то этот перпендикуляр GF разделит диаграмму на две части, совершенно аналогичные диаграмме, рассмотренной выше. Линия НА попрежнему является линией насыщения льдом, AGE - кривая растворимости кристаллогидрата состава F, и поэтому области AGR и GQE есть поля кристаллизации кристаллогидрата. [42]
Однако зависимость растворимости кристаллогидратов сульфата тория от температуры иная, чем у церия. На рис. 30 приведены кривые, из которых видно, что при повышении температуры примерно до 45 С растворимость устойчивого девятивод-ного кристаллогидрата возрастает; при температурах выше 45 С устойчивой является четырехводная форма, растворимость которой при дальнейшем увеличении температуры уменьшается. [43]
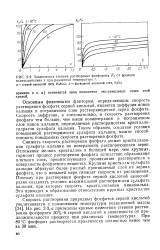 |
Зависимость степени растворения фосфорита К. от времени. [44] |
Основным физическим фактором, определяющим скорость растворения фосфата серной кислотой, является диффузия ионов кальция в пограничном слое растворяющегося зерна фосфата. Скорость диффузии, а следовательно, и скорость растворения фосфата тем больше, чем выше концентрация в пограничном слое ионов кальция, определяемая растворимостью кристаллогидратов сульфата кальция. [45]
Страницы: 1 2 3 4