Растворимость - образующийся осадок
Cтраница 2
Теперь концентрация ионов серебра в растворе, от которой зависит величина электродного потенциала, определяется растворимостью образующегося осадка. До тех пор пока весь комплекс не превратится в осадок, потенциал системы остается неизмененным. После этого дальнейшее прибавление ннтрата серебра приводит к возрастанию потенциала. [16]
 |
Кривая потенциометрического титрования цианид-ионов раствором нитрата серебра по методу комплексообразования. [17] |
Теперь концентрация ионов серебра в растворе, от которой зависит величина электродного потенциала, будет определяться растворимостью образующегося осадка. [18]
При определении истинной точки эквивалентности в ряде случаев необходимо вносить поправку на диффузионный ток, получающийся за счет растворимости образующегося осадка. [19]
В случае заметной растворимости образующегося осадка ход кривой кондуктометриче-ского титрования вблизи эквивалентной точки будет сильно искажен ( рис. 81), так как здесь растворимость образующегося осадка максимальна. [20]
Для предотвращения выпадения слишком мелких осадков необходимо: а) вести осаждение из разбавленных растворов солей разбавленным раствором осадителя; б) приливать раствор осадителя медленно, по каплям, постоянно перемешивая раствор стеклянной палочкой; в) повышать растворимость образующегося осадка, ведя осаждение из горячего раствора или прибавляя тот или иной реактив, повышающий растворимость образующегося соединения. Эта повышенная растворимость должна быть в дальнейшем понижена охлаждением раствора или добавлением избытка осадителя, или каким-либо другим способом. [21]
В этом отношении процесс комплексообра-зования аналогичен процессу осаждения. Осаждение происходит тем полнее, чем меньше растворимость образующегося осадка. [22]
На рис. 111 приведены кривые потенциометрического титрования нитрата серебра раствором хлорида. В точке эквивалентности наблюдается резкий скачок потенциала. Величина скачка потенциала зависит от растворимости образующегося осадка. [23]
Органические осадители в большинстве случаев малорастворимы в воде. Поэтому их часто приходится применять в виде растворов в спирте, ацетоне и других неводных растворителях. Однако присутствие органических растворителей при осаждении повышает растворимость образующегося осадка и делает осаждение менее полным. Чтобы избежать этого, не следует прибавлять большого избытка осадителя. [24]
Органические осадители в большинстве случаев трудно растворимы в воде. Поэтому их часто приходится применять в виде растворов в спирте, ацетоне и других неводных растворителях. Однако присутствие этих растворителей при осаждении повышает растворимость образующегося осадка и делает осаждение менее полным. Чтобы избежать этого, не следует прибавлять большого избытка осадителя. [25]
 |
Кривая потенциометрического титрования нитрата серебра раствором хлорида по методу осаждения.| Кривая потенциометри. [26] |
На рис. 198 приведена кривая потенциометрического титрования нитрата серебра ок-салатом. При этом титровании кривая несимметрична и скачок потенциала значительно меньше, чем в первом случае. Величина скачка потенциала зависит прежде всего от растворимости образующегося осадка. [27]
Органические осадители в большинстве случаев трудно растворимы в воде. Поэтому их часто приходится применять в виде растворов в спирте, ацетоне и других неводных растворителях. Однако присутствие этих растворителей при осаждении повышает растворимость образующегося осадка и делает осаждение менее полным. Чтобы избежать этого, не следует прибавлять большого избытка осадителя. [28]
 |
Кривые силы тока при замедленном образовании осадка при титровании кальция раствором ферроцианида калия. [29] |
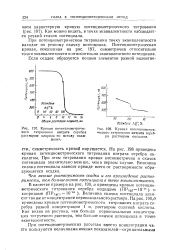
Однако практически это неудобно, так как требует большой дополнительной затраты времени на проявление снимка, ничем не оправдываемой в связи с тем, что точность отсчета силы тока при автоматической записи в некоторых случаях может быть даже меньше, чем при обычной визуальной регистрации показаний гальванометра. Дело в том, что при титровании по методу осаждения ( по типу кривой б) необходимо считаться не только с растворимостью образующегося осадка, но и со скоростью его образования: если осадок образуется не мгновенно, то в первый момент после добавления титрующего раствора сила тока возрастает пропорционально количеству добавленного реактива и затем постепенно уменьшается по мере того, как происходит связывание добавленного реактива и образование осадка. В таких случаях не следует регистрировать первый, бросковый ( пользуясь выражением Е. М. Скобца), ток, а необходимо выждать, пока между раствором и осадком не установится равновесие, после чего сила тока примет постоянное значение. Верхняя кривая соответствует значениям броскового тока, нижняя - силе тока после выжидания. Обычно выжидать приходится не больше 0 5 мин. [30]
Страницы: 1 2 3