Донорный растворитель
Cтраница 3
Исследование растворов хлорида железа ( Ш) в этих сильных донорных растворителях показало, что кроме донорного числа растворителя следует учитывать влияние и других факторов. N-Метилацетамид не способствует образованию иона FeCl -, этот ион неустойчив также в воде и в спиртах. [31]
Катионы металлов, проявляя кислотные свойства, координируясь с молекулами донорного растворителя, образуют сольваты. [32]
В растворителях со средней донорной силой может происходить замещение молекулами донорного растворителя одного или большего числа ионов хлора в некоторых слабых акцепторных хлоридах. [33]
Поскольку теплота процесса сольватации является характеристикой прочности сольватации данного акцептора различными донорными растворителями, калориметрические измерения теплот сольватации предоставляют простую возможность оценки донорной способности. [34]
Уменьшение отношения третичный / первичный при повышении температуры реакции в донорном растворителе отражает снижение стабильности л-комплекса. [35]
При растворении акцепторного соединения АХД, например SbClu, в донорном растворителе D по схеме [1] происходит образование сольватного комплекса. Сольватный комплекс может затем реагировать с конкурирующим лигандом L. Реакции замещения такого типа могут осуществляться а) при добавлении более сильного, чем растворитель, донора или б) благодаря смещению равновесия вследствие различий в летучести, растворимости или при добавлении большого избытка замещающего донора. Образование аммиакатов некоторых переходных металлов в водном растворе осуществляется в соответствии с пунктом а) и обусловлено более сильными донорными свойствами аммиака по сравнению с водой, хотя вода благодаря ее меньшей летучести по сравнению с аммиаком может быть в избытке. [36]
Энергия стадии в на рис. 44 может быть качественно оценена по способности донорного растворителя координировать с растворенным веществом. [37]
Кислоты, содержащие полярную связь Н - А, при взаимодействии с донорным растворителем Д образуют ионные пары ДН А -, которые в свою очередь могут диссоциировать в полярных средах. [38]
Растворители, способные образовывать координационную связь с акцепторами электронных пар, называются донорными растворителями. В противоположность им растворители, образующие координационную связь с донорами электронных пар, Гутман называет [40, 41] акцепторными растворителями. [39]
К сожалению, не измерены до норные числа формамида и ацет-амида - этих сильных донорных растворителей, которые создают благоприятные условия для образования прочных комплексов. [40]
Сольватация анионов акцепторными растворителями обычно осуществляется в меньшей степени, чем сольватация катионов донорными растворителями. [41]
Галогениды и Zn и Cd вполне растворимы в спирте, ацетоне и в других донорных растворителях, и в некоторых случаях возможно образование продуктов присоединения. [42]
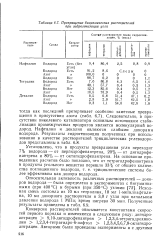 |
Превращение бициклических растворителей при гидрогенизации угля. [43] |
Исходная смесь состояла из 10 мл тетралина, 10 мл 1-метилнафтали-на, 10 мл донорного растворителя и 3 0 г угля при начальном давлении водорода 1 МПа; время нагрева 30 мин. [44]
Под действием света с длиной волны 360 - 400 ммк растворы ге-хлоранила в таких донорных растворителях, как тетрагидрофуран, диоксан и некоторые алкилбен-золы, также дают сигнал ЭПР. При использовании в качестве акцепторов полинитроароматических соединений, например симм-тринитробензола в тетрагидрофуране, поглощение исчезает медленнее и время исчезновения зависит от температуры. Тот же результат получен при использовании в качестве акцепторов n - хлоранила и нитроароматических соединений. [45]
Страницы: 1 2 3 4