Кислый растворитель
Cтраница 1
Кислые растворители применяются в основном для усиления основных свойств очень слабых оснований. Чтобы еще полнее использовать действие растворителя, необходимо в качестве титрующего средства использовать как можно более сильную кислоту. [1]
Кислые растворители в силу своих сильных протогенных свойств оказывают существенное влияние на диссоциацию кислот и оснований. В среде этих растворителей уменьшается число веществ, проявляющих кислые свойства, и увеличивается число веществ, проявляющих основные свойства. Следовательно, в среде протогенных растворителей усиливается диссоциация электролитов по типу оснований. [2]
Кислый растворитель, содержащий 75 мл изопропилового спирта, 25 мл дистиллированной воды, 5 г трихлоруксусной кислоты, 0 25 мл 25 % - ной аммиачной воды. [3]
Кислые растворители ( безводная уксусная кислота, жидкий фтористый водород и др.), отличающиеся склонностью отдавать свои протоны, усиливают ионизацию по типу оснований. [4]
Кислый растворитель ( см. в таб-ице колонку НСООН) сдвигает величины потенциа-ов в отрицательную сторону, основные растворители в колонках N2H4 и NH3) - в положительную. [5]
 |
Классификация растворителей ( по Бренстеду. [6] |
Кислые растворители относительно малочисленны. Амфотерные растворители часто подразделяют на кислые амфотерные и основные амфотерные, исходя из преобладающих свойств. [7]
Кислые растворители в силу своих сильных протогенных свойств оказывают существенное влияние на диссоциацию кислот и оснований. В среде этих растворителей уменьшается число веществ, проявляющих кислые свойства, и увеличивается число веществ, проявляющих основные свойства. Следовательно, в среде протогенных растворителей усиливается диссоциация электролитов по типу оснований. [8]
 |
Классификация растворителей ( по Бренстеду. [9] |
Кислые растворители относительно малочисленны. Амфотерные растворители часто подразделяют на кислые амфотерные и основные амфотерные, исходя из преобладающих свойств. [10]
Из кислых растворителей наиболее широко используются в качестве среды для титрования оснований безводная уксусная кислота, гликоли и их смеси с другими растворителями. [11]
Самым распространенным кислым растворителем является ледяная уксусная кислота, применяемая в сочетании с титрантом - хлорной кислотой в уксусной кислоте. Эту систему применяют для определения оснований с рКь в воде 12 и ниже. [12]
В кислых растворителях ( УК, УА, МК) возможно титрование оснований любой силы в воде. [13]
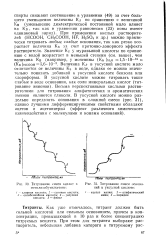 |
Титрование смеси кислот в метилизобутилкетоне.| Титрование смеси оснований в уксусной кислоте. [14] |
При применении кислых растворителей ( НСООН, СН3СООН, HF, H2SO4 и др.) можно практически титровать любые слабые основания, так как резко возрастает величина Кв за счет протонно-донорного эффекта растворителя. Ks в воде, однако ее можно значительно понизить добавкой к уксусной кислоте бензола или хлороформа. Весьма перспективными кислыми растворителями для титрования алифатических и ароматических аминов являются гликоли. [15]
Страницы: 1 2 3 4