Кислый растворитель
Cтраница 3
Перед хроматографическим анализом кислый растворитель должен быть полностью удален с пластинки. [31]
Серная кислота - наиболее кислый растворитель из всех систематически исследованных до настоящего времени. Диэлектрическая постоянная серной кислоты, хотя, по-видимому, и не определялась до настоящего времени, безусловно больше диэлектрической постоянной любого из известных растворителей. [32]
В случае применения кислых растворителей, необходимо длительное выветривание хроматограмм в токе холодного воздуха для удаления кислоты с хроматограммы. [33]
Равным образом в кислых растворителях наблюдается сильное влияние растворителя на основания. [34]
В то время как кислые растворители способны увеличивать силу оснований, на кислоты они оказывают обратное действие, уменьшая их силу. Так, соляная кислота, являющаяся сильной кислотой в воде, лишь частично диссоциирует в ледяной уксусной кислоте; кислоты, являющиеся слабыми в воде, в кислом растворителе становятся еще более слабыми. [35]
Таким образом, применение кислых растворителей значительно улучшает условия титрования оснований и делает возможным распространение этого метода на титрование очень слабых оснований. [36]
Вторая группа носит название кислых растворителей. У них способность к выделению протона значительно превышает способность к его присоединению. [37]
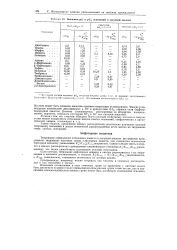 |
Значения рК и р т оснований в уксусной кислоте. [38] |
Таким образом, применение кислых растворителей значительно улучшают условия титрования оснований и делает возможным распространение этого метода на титрование очень слабых оснований. [39]
Вторая группа носит название кислых растворителей. У них способность к выделению протона значительно превышает способность к его присоединению. Естественно, что к этой-группе относятся кислоты: уксусная, масляная, муравьиная и другие. [40]
Таким образом, применение кислых растворителей значительно улучшает условия титрования оснований и делает возможным распространение этого метода на титрование очень слабых оснований. [41]
Вторая группа носит название кислых растворителей. У них способность к выделению протона значительно превышает способность к его присоединению. [42]
Хроматограммы, полученные с кислыми растворителями, следует предварительно нагревать 60 мин при 120 для удаления уксусной кислоты. [43]
В настоящее время самым распространенным кислым растворителем является уксусная кислота, применяемая в сочетании с хлорной кислотой как титрантом. При титровании хлорной кислотой в безводной уксусной кислоте были получены четкие точки перегиба для очень слабых оснований, которые не удается оттитровать в воде. [44]
Соли органических кислот в кислых растворителях титруются по вытеснению минеральной кислотой как основания. [45]
Страницы: 1 2 3 4