Электронодонорный растворитель
Cтраница 1
Электронодонорные растворители специфически сольватируют катионы щелочных металлов, в частности натрия и калия. При этом нарушается их взаимодействие с анионами, благодаря чему сила последних как оснований резко повышается. [1]
Электронодонорные растворители ( диметилформамид, триэтиламин и др.) и наличие в мономере электроноакцепторных групп ( акрилоиитрил) способствуют полимеризации по анионному механизму. [2]
Эффект электронодонорного растворителя или добавок заключается в снижении электронодефицитности реагентов и в то же время в усилении их сходства с карбанионами и, таким образом, и их нуклеофильности и основности. Последний эффект, в частности, проявляется в промотировании процесса металлирования добавками, такими, как ТМЭДА ( см. разд. В предельном случае в растворе, по-видимому, присутствуют ионные пары карбанионов и сольватированных ионов лития, хотя в твердом состоянии литий и карбанион тесно ассоциированы, даже если последний делокализован. [3]
Использование нейтральных электронодонорных растворителей затрудняет протонный обмен и способствует спин-спиновому расщеплению гидроксильного и а-углеродного протонов. [4]
 |
Схема установки для проведения реакции стационарно-проточным методом.| Прибор для измерения скорости быстрых реакций полимеризации. [5] |
Полимеризация ряда мономеров в электронодонорных растворителях с большой сольватирующей способностью протекает с высокой скоростью как из-за значительной реакционноспособности активных центров вследствие сольватации противоиона, так и из-за высокой действующей концентрации активных центров вследствие отсутствия их ассоциации. [6]
Однако разложение ГПК в среде электронодонорного растворителя, каким является диметилформа-мид ( ДМФА), в присутствии соединений молибдена не исследовалось. [7]
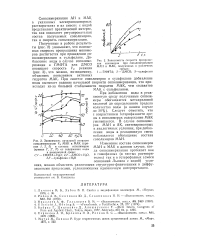 |
Зависимость начальной скорости сополимеров МАН. [8] |
Сополимеризация АН и МАК в указанных электронодонорных растворителях и их смесях с водой представляет практический интерес, так как позволяет регулировать как состав получаемых сополимеров, так и скорость сополимеризации. [9]
При выполнении последнего условия равновесная концентрация электронодонорного растворителя в формуле ( 1) заменяется исходной концентрацией Св. Соотношение ( 1) не содержит концентрации бутилацетилена, что удобно при работе с газообразными и дефицитными соединениями. [10]
Отметим, что закономерности протекания радикальных реакций в присутствии электронодонорных растворителей часто оказываются сложнее, чем в присутствии соединений, сольватирующих радикал за счет водородной связи. Этот эффект противоречит представлению о том, что комплексообразование радикалов с электро-нодонорными растворителями должно резко снижать их реакционную способность. [11]
Расщепление силоксановой связи водой облегчается при проведении реакции в электронодонорном растворителе и при замене метальных групп в полидиметилсилоксанах на атомы водорода или электроноакцепторные группы. [12]
Соединения с межмолекулярной Н - связью лучше растворяются в электронодонорных растворителях, которые могут разрушать уже имеющиеся межмолекулярные связи и образовывать с растворенным веществом новые Н - связи. [13]
Отметим, что особенно сильная чувствительность реакционной способности Cl-радикала к влиянию электронодонорных растворителей ( в данном случае я-доноров) связана, вероятно, со значительным сродством этого радикала к электрону. Например, значения энергии сродства к электрону таких радикалов, как СНз, СвН5О, НОз и С1, равны соответственно25 27 70 и 88 ккал / моль. Естественно, что в гемолитических реакциях с участием метильного или феноксильного радикалов влияние электронодонорных растворителей должно сказываться меньше, чем в реакциях хлорирования. [14]
Реакция алюминийтриалкилов с щелочными металлами проходит гладко в инертных и сольватирующих электронодонорных растворителях, но может идти и без растворителей. [15]
Страницы: 1 2 3 4