Изученный растворитель
Cтраница 2
Заметно влияние размеров и электронной поляризуемости анионов в изученных растворителях. Так, например, при переходе от хлоридов к бромидам, иодчдам разности ( ИАЯ СОЛЬВ - 2АЯ ГИДР) растут. Повышение температуры уменьшает эту разницу. [16]
Согласно полученным результатам, НТ1С14 и НСЮ4 могут экстрагироваться изученными растворителями как по гидроксоние-вому, так и по оксониевому механизмам. [17]
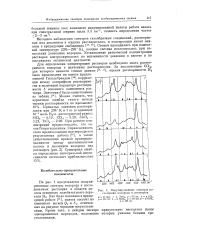 |
Индуцированные спектры поглощения водорода в растворах. [18] |
Для определения концентрации растворов необходимо знать растворимость водорода в изученных растворителях. За исключением СС14, для которого имеются точные данные [16 17], оценка растворимости Н2 была произведена на основе предложенной Гильдебрандом [18] корреляции между логарифмом растворимости и величиной параметра растворимости б основного компонента раствора. При расчете концентраций предполагалось, что закон Генри выполним. [19]
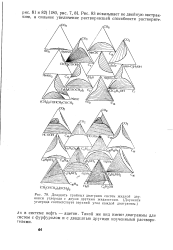 |
Двадцать тройных диаграмм систем жидкой двуокиси углерода с двумя другими жидкостями. ( Двуокиси углерода соответствует верхний угол каждой диаграммы. [20] |
Такой же вид имеют диаграммы для систем с фурфуролом и с двадцатью другими изученными растворителями. [21]
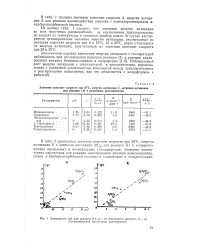 |
Зависимость Ig. для реакции ( 1. а - от дипольного момента. б - от диэлектрической постоянной растворителя. [22] |
Из данных табл. 1 следует, что значения энергии активации во всех изученных растворителях, за исключением трихлорэтилена, не зависят от температуры в пределах ошибок опыта. В случае растворителя трихлорэтилена значения энергии активации, рассчитанные из значения констант скорости при 0 и 15 С, 15 и 25 С, резко отличаются от энергии активации, рассчитанной из значения констант скорости при 25 и 35 С. [23]
Основные уравнения теории диффузного слоя применимы для количественного описания свойств границы висмута с изученными растворителями. Этот результат свидетельствует о том, что в этих растворителях соли Кр, 1ЛС1О4 или NaClO4 поверхностно-неактивны и в исследованном интервале концентраций в первом приближении можно пренебречь ассоциацией ионов в объеме раствора. [24]
Высокие значения поправочных коэффициентов при 150 и 250 потеряли бы значение вследствие малого числа изученных растворителей, если бы не тот факт, что при 200 и 300 были получены хорошие соотношения с большим числом растворителей. [25]
Как уже указывалось, реакция бензилмеркурх / горида с иодом в отсутствие иодид-ионов во всех изученных растворителях, в том числе и в полярных, осуществляется по радикальному механизму. Интересно, что даже такой растворитель, как ДМСО, не составляет исключения, хотя с более реакционноспособными соединениями реакция в нем осуществляется по мономолекулярному механизму типа SEl с предварительной ионизацией ртутноорганического соединения. Без освещения реакция протекает чрезвычайно медленно, поэтому ее изучали при облучении реакционной смеси стабилизованным источником света. Для реакции бен-зшшеркурхлсрида с иодом в неполярном растворителе СС14 найдено, что константа скорости реакции формально удовлетворяет уравнению для реакций первого порядка и сохраняет свое значение ( по иоду) при варьировании исходных концентраций реагентов, в том числе и при многократном избытке ртутноорганического соединения. [26]
С ъ), триметилалкиламмоний хлорид ( 20), диметилалкилбензиламмоний хлорид ( 22) ] с изученными растворителями, имеющими относительно высокую диэлектрическую проницаемость [17] ( диэтиловый эфир, нитробензол, хлороформ), практически полностью экстрагируют цинк из роданидных растворов. Вторичные амины ( ме-тилоктадециламин, хинолин) в меньшей степени экстрагируют цинк. И, наконец, первичные амины ( дециламин, бутиламин, октадециламин) экстрагируют цинк хуже вторичных, третичных и четвертичных оснований. [27]
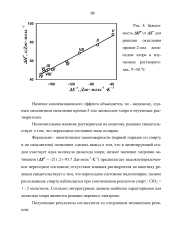 |
Зависимость АН от AS для. [28] |
Наличие компенсационного эффекта объясняется, по - видимому, единым механизмом окисления пропан-2 - ола диоксидом хлора в изученных растворителях. [29]
Удивительно, что соответствие выхода с внутренним давлением столь хорошее, если принять во внимание, что в число изученных растворителей были включены широко разнообразные химические соединения, многие из которых были очень полярны. [30]
Страницы: 1 2 3 4