Гидроксилсодержащий растворитель
Cтраница 2
В гидроксилсодержащих растворителях гипогалогениты могут также служить источником положительного галогена, что приводит к электрофильному присоединению к алкенам и замещению аренов. [16]
В гидроксилсодержащих растворителях соотношения между механизмами и продуктами реакций не могут считаться удовлетворительно выясненными. [17]
Дифференцирующий эффект гидроксилсодержащих растворителей объясняется как уменьшением е, ( по сравнению с ен2о) и кислотности растворителей, так и размером и природой их радикалов. Исследуя дифференцирующее действие кислородсодержащих растворителей ( в том числе и спиртов), Дулова [310] пришла к выводу, что рД карбоновых кислот в алифатических спиртах возрастают с уменьшением е растворителей больше, чем р / С фенолов в тех же растворителях, что объясняется различием в ассоциации их ионов. [18]
Слорид-ион в гидроксилсодержащих растворителях сильно соль - Йатирован и проявляет свойства более слабого нуклеофильного аген-по сравнению с бромид - и йодид-ионами. Поэтому для получе-алкилхлоридов при взаимодействии первичных спиртов с со-ой кислотой используют электрофильный катализатор - 1ДНЫЙ хлорид цинка. Смесь соляной кислоты и хлорида цин-носит название реактива Лукаса. [19]
 |
Значения частот СО-групп в спектрах растворов карбоновых кислот [ 10 % ( мол. ]. [20] |
Почти во всех гидроксилсодержащих растворителях относительная интенсивность спектров флюоресценции недиссоциированной салициловой кислоты одинакова, а в растворителях, не содержащих гидроксильных групп - в дифференцирующих растворителях, также одинакова, но отличается от предыдущей. [21]
Почти во всех гидроксилсодержащих растворителях относительная интенсивность спектров флюоресценции недиссоциированной салициловой кислоты одинакова, а в растворителях, не содержащих гидроксильных групп - - в дифференцирующих растворителях, также одинакова:, но отличается от предыдущей. [22]
Хлорид - ион в гидроксилсодержащих растворителях сильно сольватироваи и проявляет свойства более слабого нуклеофильного агента по сравнению с бромид - и йодид - ионами. Поэтому для получения алкилхлоридов при взаимодействии первичных спиртов с соляной кислотой используют электрофильный катализатор - безводный хлорид цинка. Смесь соляной кислоты и хлорида цинка носит название реактива Лукаса. [23]
 |
Влияние ассоциации лс-фторбензола. [24] |
Как видно, в гидроксилсодержащих растворителях происходит большее смещение сигнала 19F в сторону слабых полей по сравнению со смещением в инертных растворителях. [25]
Он очень чувствителен к действию гидроксилсодержащих растворителей и вообще реагирует с нуклеофильными реагентами гораздо легче, чем хлоранил. Например, все четыре его атома галоида способны заменяться на аминогруппы. Реакцию с первичными или вторичными аминами можно провести таким образом, что получается 2 5-диамин, который при взаимодействии с тем же или другим амином превращается в тет-раамин Тетрааминобензохинон удобнее всего получать реакцией фторанила с фталимидом калия и расщеплением образовавшегося продукта гидразином. [26]
Он очень чувствителен к действию гидроксилсодержащих растворителей и вообще реагирует с нуклеофильными реагентами гораздо легче, чем хлоранил. Например, все четыре его атома галоида способны заменяться на аминогруппы. Реакцию с первичными или вторичными аминами можно провести таким образом, что образуется 2 5-диамин, который при взаимодействии с тем же или другим амином превращается в тет-раамин. [27]
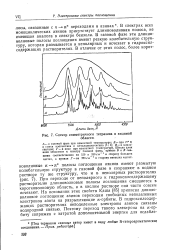 |
Спектр симметричного тетразина в видимой области. [28] |
При переходе от неполярного к гидроксилсодержащему растворителю длинноволновые полосы поглощения смещаются в коротковолновую область, а в кислом растворе они часто совсем исчезают. На основании этих свойств Каша [85] приписал длинноволновое поглощение азинов переходам свободных неподеленных электронов азота на разрыхляющие я-орбиты. В гидроксилсодер-жащих растворителях неподеленные электроны азинов связаны водородной связью. [29]
При атаке отрицательными ионами в гидроксилсодержащих растворителях и ZA, и 1 - LT отрицательны, так что наклон графика зависимости Еа от i / D должен быть положительным. Как правило, это и наблюдается на опыте, хотя получаемые из таких графиков оценки для г обычно слишком малы, например, 0 73 А для реакции СН3Вг I - СН31 - - Вг - в различных растворителях. [30]
Страницы: 1 2 3 4