Расчет - изменение - энтропия
Cтраница 1
Расчет изменения энтропии ( ASr) часто облегчается наличием справочных значений Sr компонентов реакции. [1]
Расчеты изменения энтропии в реальных случаях облегчаются тем, что практически обратимыми являются такие процессы, как фазовые превращения и нагревание-охлаждение. [2]
Расчеты изменения энтропии проводятся при помощи уравнения dS 8q / T. При этом для получения правильных результатов необходимо, чтобы процесс, при помощи которого по калориметрическим данным определяется AS, был обратимым. [3]
Расчеты изменения энтропии в реальных случаях облегчаются тем, что практически обратимыми являются такие процессы, как фазовые превращения и нагревание - охлаждение. [4]
Расчеты изменения энтропии проводятся при помощи уравнения dS 6Q / T. При этом для получения правильных результатов необходимо, чтобы процесс, при помощи которого по калориметрическим данным определяется AS, был обратимым. [5]
Расчет изменения энтропии обожженного образца каолина в области дегидратации выполняется в два этапа. [6]
Рассмотрим расчет изменения энтропии в некоторых процессах. [7]
Для расчета изменения энтропии, вызванного процессами теплопроводности и диффузии, рассмотрим простейший пример. Для того чтобы сначала исключить изменение энтропии, вызванное перемешиванием различных молекул, допустим, что эти объемы отгорожены подвижной и теплопроницаемой перегородкой. [8]
Для расчета изменения энтропии AS необходимо знать температурную зависимость молярной теплоемкости в соответствующем температурном интервале. [9]
Для расчета изменения энтропии системы через вероятности состояний очень часто используется метод Колмогорова. [10]
Для расчета изменения энтропии реальных газов с изменением давления приходится пользоваться или подходящим уравнением состояния, с достаточной степенью точности описывающим поведение газа, или непосредственными измерениями. [11]
Для расчета изменения энтропии внешней среды следует предположить, что вода находится в тепловом контакте с большим резервуаром, имеющим температуру - 10 С. При замерзании воды происходит выделение теплоты ( теплота плавления при - 10 С равна 313 9 Дж / г), которая поглощается резервуаром без заметного изменения его температуры. [12]
При расчете изменений энтропии необходимо тщательно учитывать фазовые переходы. [13]
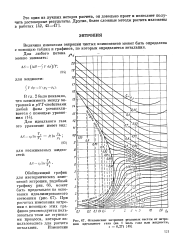 |
Отклонение энтропии реальных систем от энтропии идеального газа ( на 1 моль газа или жидкости. [14] |
При расчетах изменения энтропии с помощью этих графиков рекомендуется пользоваться теми же ступенями процесса, которые использовались для расчета энтальпии. [15]
Страницы: 1 2 3