Расчет - константа - равновесие
Cтраница 3
Способ расчета констант равновесия [, с помощью уравнения (7.22) аналогичен способу расчета в методе растворимости. [31]
Для расчета констант равновесия этих реакций потребовалось уточнение стандартных энтальпий монохлорида галлия и двухатомного мышьяка, величины которых приводятся в литературе с большим разбросом. С этой целью экспериментально изучался состав пара мышьяка и равновесия в системе галлий - хлор методом кварцевого мембранного манометра. [32]
Метод расчета констант равновесия из данных о нормальных ред-окс-потенциалах применим также и к определению возможности реакции дисмутации. [33]
Для расчета константы равновесия должны быть следующие данные: количества взятых веществ и суммарная концентрация кислоты в равновесной смеси. Ход расчета несколько различен для опытов по образованию этилацетата из спирта и уксусной кислоты и для опытов по омылению этого эфира водой. [34]
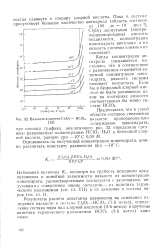 |
Вязкость в системе С12О7 - НС1О4. [35] |
Результаты расчета константы равновесия на основании измерения вязкости в системе С12О7 - НСЮ4 ( 1 - й метод), определение состава пара над хлорной кислотой ( 2 - й метод) и изучение кинетики термического разложения НСЮ4 ( 3 - й метод) даны ниже. [36]
Для расчета константы равновесия Кр необходимо иметь значения приведенного изобарного потенциала ( G - Ho) jT при разных температурах для всех веществ, участвующих в реакции, и тепловой эффект реакции Д / / 0 при абсолютном нуле. [37]
Для расчета константы равновесия метана задают значение летучести метана при данных давлении ихгемпературе. [38]
Для расчета констант равновесия неидеальных систем необходимо знать коэффициенты активности обмениваемых ионов в твердой фазе и в растворе ( стр. Коэффициент распределения представляет собой отношение числа миллиграмм-эквивалентов иона, сорбированного 1 г ионообменника, к числу миллиграмм-эквивалентов этого иона, находящегося в 1 мл раствора в равновесных условиях. Таким образом, коэффициент распределения непосредственно характеризует степень извлечения ионообменником иона из раствора. [39]
При расчете константы равновесия этой гетерогенной реакции ( константы обмена) следует учитывать коэффициенты активности веществ в растворе и в сорбенте. [40]
При расчете констант равновесия можно выразить действующие массы реагентов через массу только одного из участников процесса, так как количественные соотношения между веществами определяются стехио-метрическим уравнением реакции. [41]
При расчете констант равновесия по четвертому методу дополнительно использовались сведения, полученные другими исследователями. Причем точность дополнительных параметров ( летучесть компонентов, коэффициент активности и др.), задействованных в расчетах не указывается, однако отмечаются их различия у разных исследователей. Наибольшее несоответствие отмечается у пропана и изо - и нормального бутанов. [42]
При расчете констант равновесия в зависимости от давления учтено влияние критических параметров. [43]
При расчете констант равновесия, например гетерогенных жидких систем или крепких растворов, часто возникают серьезные трудности. Кроме состояния равновесия, иногда требуется найти скорость протекания реакции на различных стадиях процесса. Эта величина зависит от таких физических параметров, как вязкость, скорость диффузии, дисперсность и пр. [44]
При расчете константы равновесия этой гетерогенной реакции ( константы обмена) следует учитывать коэффициенты активности веществ в растворе и в сорбенте. [45]
Страницы: 1 2 3 4