Расчет - константа - скорость - реакция
Cтраница 1
Расчет констант скорости реакции k между смолой и оксидным катализатором показал, что для этой медленной реакции величина А имеет низкие значения, например, для катализатора Pt на А12О3 ( АП-64) k 0 275 ч при температуре термообработки 300 С. [1]
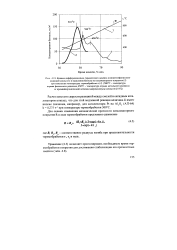 |
Кривые дифференциально-термического анализа полиметилфенилсило. [2] |
Расчет констант скорости реакции k между смолой и оксидным катализатором показал, что для этой медленной реакции величина k имеет низкие значения, например, для катализатора Pt на А12О3 ( АП-64) k 0 275 ч 1 при температуре термообработки 300 С. [3]
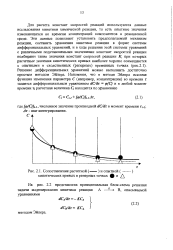 |
Сопоставление расчетной ( - . - и опытной ( - - - - - . [4] |
Для расчета констант скоростей реакций используются данные исследования кинетики химической реакции, то есть опытные значения изменяющихся во времени концентраций компонентов в реакционной среде. [5]
Для расчета константы скорости реакции димеризации необходимо определить обратимый потенциал полуволны системы Red / Ox. Это серьезная задача, и в случае быстрых химических реакций ее часто трудно решить. Теоретически при значительном уменьшении кинетического параметра X можно так сократить процесс, что последующая реакция уже не вызовет изменений концентрации формы Red. [6]
Результаты расчета констант скоростей реакций алкилирования n - ксилола при 100 С, количестве катализатора, равном 0 01 моля хлористого алюминия на моль ксилола, приведены ниже ( с -): k 3 22 X Х10 - 4; kz 2 68 - Ю-4; Й3 0 54 10 -; kt 2 35 - Ю-4. Поскольку третье и четвертое замещения проходят с большим трудом, расчет констант на молекулярном уровне дал более предпочтительные результаты. [7]
Для расчета констант скорости реакций первого порядка при разложении метана были использованы данные нескольких исследователей. [8]
 |
Определение координат центра тя-жести молекулы СН2СН2. [9] |
При расчете константы скорости реакции методом активированного комплекса определение статистических сумм для поступательного движения не представляет затруднений. Определение же вращательных статистических сумм требует знания моментов инерции. [10]
При расчете констант скоростей реакций использовалось полученное ранее экспериментальное распределение продуктов алкилирования. Расчет сделан для трех изомеров ксилолов. [11]
Ниже приводится расчет константы скорости реакции этерифи-кации через 30 мин для смеси гексанол-1 - н-валериановая кислота. [12]
На основании расчета констант скоростей реакции Меервейн полагал, что процесс течет мономолекулярно, однако в дальнейшем было выяснено, что он сложнее и имеет различный, обычно более высокий порядок реакции ( стр. [13]
На основании расчета констант скоростей реакции Меервейн полагал, что процесс течет мономолекулярно, однако в дальнейшем было выяснено, что он сложнее и имеет различный, обычно более высокий порядок реакции ( стр. [14]
 |
Определение координат центра тяжести молекулы СН2СН2. [15] |
Страницы: 1 2 3 4