Расчет - электронная плотность
Cтраница 2
Эти соображения и определяют количество точек ячейки, для которых следует производить расчет электронной плотности. Подразделение элементарной ячейки на интервалы, значительно меньшие, чем 0 3 А, не имеет смысла. Но нельзя также допускать и значительно больших интервалов, так как это может привести к потере некоторых максимумов. Примем за основу требование, чтобы самый большой интервал между соседними точками был равен приблизительно 0 3 - 0 35 А. В структурах средней сложности линейные размеры элементарной ячейки лежат в пределах 8 - 16 А, а следовательно, самое длинное линейное сечение ячейки - пространственная диагональ ее - имеет длину в 14 - 28 А. [16]
Более того, легкость окисления боковой цепи может быть объяснена на основании расчетов относительной электронной плотности НСМО на ароматическом атоме углерода, соседнем с метиль-ной группой, по сравнению с другими положениями в катион-радикале. Относительная электронная плотность НСМО в положении, соседнем с метильной группой, в n - метиланизоле выше, чем аналогичная величи-на для jn - метиланизола. Цианид-ион атакует ароматический атом углерода, соседний с метильной группой, так как электронная плотность НСМО на нем наибольшая, и отщепляет протон из бензильного положения катион-радикала. [17]
Электрофильная атака на атомы углерода цикла протекает сложно; попытки корреляции между расчетами электронной плотности, механизмом реакции и экспериментальными результатами большого успеха не имели. [18]
Кроме того, на любой стадии уточнения после операции 5 может быть подключен расчет электронной плотности по всем клеткам элементарной ячейки. [19]
Обычно присоединение первичного иона К к мономеру происходит по месту наибольшей электронной плотности в молекуле, что согласуется с кванто-во-химическими расчетами относительной электронной плотности на атомах углерода алкенильной группы мономера. [20]
В результате суммирования ряда Фурье первого приближения получаем значительно менее правильное представление о действительном распределении электронной плотности в ячейке, чем в случае центросимметрической структуры, при расчете электронной плотности которой ошибочно определяются лишь некоторые, сравнительно малые по величине коэффициенты ряда. Последовательное улучшение картины по мере пересчета ряда также достигается гораздо медленнее, так как предыдущее, более грубое приближение к истине со всеми ошибками участвует в построении последующего приближения более ощутимо. [21]
Это говорит о частичной заселенности этих центров двумя или большим количеством атомов, находящихся на расстоянии примерно 0 5 А и плохо разрешающихся в рентгенограммах. Расчет электронной плотности в местах Sj для Na дает 33 2 1 6 атома, что свидетельствует о полной заселенности этих мест. При расчете на азот центр содалитовой ячейки оказывается также полностью заселенным, а в местах S, , размещаются либо 14 9 1 3 атома кислорода, либо 10 8 0 9 атома натрия. В картах распределения электронной плотности регистрируется плотность в больших полостях, которая может характеризовать неидентифицированные катионы. Это распределение катионов и анионов подобно ожидаемому для цеолита CaY с окклюдированным NaCl. Наличие атомов кислорода в местах S, , и атомов азота в местах U может указывать на присутствие нитратной группы в каждой содалитовой ячейке, хотя при таком расположении необходимо, чтобы в местах SJ, находились 24 атома кислорода. Присутствие нитратной группы должно, по-видимому, влиять ла положение одного из четырех атомов натрия в местах SJ, поскольку он находится в тетраэд - рическом окружении трех кислородных атомов этой группы. [22]
На практике для извлечения кислот и солей металлов используют различные кислородсодержащие нейтральные реагенты. Расчет электронной плотности на атоме кислорода группы Э О ( элемент - кислород) в многоатомных молекулах К ЭО пока невозможен. Поэтому для предсказания их экстракционной способности используют корреляции, основанные на принципе линейности свободных энергий. [23]
На следующем этапе исследования анализируют дифракционную картину и расчетным путем устанавливают взаимное расположение частиц в пространстве, вызвавшее появление данной картины. Расчет электронной плотности внутри элементарной ячейки и определение координат атомов, к-рые отождествляются с положением максимумов электронной плотности; эти данные получают анализом интенсивности дифракционных максимумов. [25]
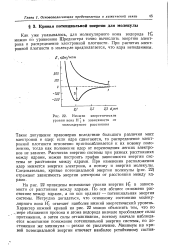 |
Низшие энергетические. [26] |
Как уже указывалось, для молекулярного иона водорода Нз можно по уравнению Шредингера точно вычислить энергию электрона и распределение электронной плотности. При расчетах электронной плотности в молекуле предполагается, что ядра неподвижны. [27]
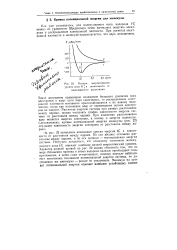 |
Низшие энергетические. [28] |
Как уже указывалось, для молекулярного иона водорода Н2 можно по уравнению Шредингера точно вычислить энергию электрона и распределение электронной плотности. При расчетах электронной плотности в молекуле предполагается, что ядра неподвижны. [29]
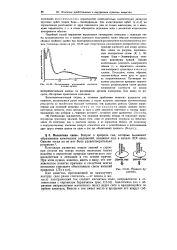 |
Распределение электронной в атоме аргона.| Правило буравчика. [30] |
Страницы: 1 2 3 4
