Расчет - равновесный состав
Cтраница 1
Расчет равновесного состава по величине KN проводится так же, как и для идеального газа, поскольку уравнение (1.56), связывающее Кк и х справедливо для любых систем. [1]
Расчет равновесных составов с помощью констант равновесия часто связан с решением уравнений третьей и четвертой степени, а также уравнений более высоких порядков. Полное решение таких уравнений во многих случаях требует трудоемких и утомительных расчетов, поэтому часто пользуются упрощенными методами. [2]
Расчет равновесного состава сводится к выбору и решению системы из одиннадцати нелинейных уравнений равновесия и материального баланса. Число уравнений баланса равно числу элементов системы, в данном случае четырем. Следовательно, помимо четырех условий баланса должны выполняться семь независимых условий химического равновесия, дающие сеть независимых уравнений. [3]
Расчет равновесных составов проводится с учетом числа молей писх, i исходных веществ, степени превращения Р основного исходного вещества и других веществ, общего давления Р, общего объема V, изменения числа молей Av в газовой или конденсированной фазах. [4]
Расчет равновесного состава сводится к выбору и решению системы из одиннадцати нелинейных уравнений равновесия и материального баланса. Число уравнений баланса равно числу элементов системы, в данном случае четырем. Следовательно, помимо четырех условий баланса должны выполняться семь независимых условий химического равновесия, дающие сеть независимых уравнений. [5]
 |
Эффективные диаметры и коэффициенты активности некоторых ионов в водных. [6] |
Расчет равновесного состава при диссоциации сильного электролита в предположении, что степень диссоциации принимается равной единице и отсутствуют химические реакции, не представляет особой сложности. Для расчета равновесных активностей необходимо знание соответствующих коэффициентов активностей. [7]
Расчет равновесного состава проведен по соотношениям, описанным в гл. [8]
Расчет равновесных составов с помощью констант равновесия часто связан с решением уравнений третьей и четвертой степени, а также уравнений более высоких порядков. Полное решение таких уравнений во многих случаях требует трудоемких и утомительных расчетов, поэтому часто пользуются упрощенными методами. [9]
Расчет равновесного состава газов представляет теоретический и практический интерес, так как позволяет определить идеальные количественные соотношения компонентов получаемого газа и установить закономерность изменения этих соотношений в зависимости от условий газификации топлива. [10]
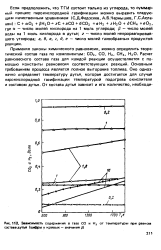 |
Зависимость содержании в газе СО и Н, от температуры при разном составе дутья ( цифры у кривых - значении 0. [11] |
Расчет равновесного состава газа для каждой реакции осуществляется с помощью константы равновесия соответствующих реакций. Основным требованием процесса является. Оно однозначно определяет температуру дутья, которая достигается для случая парокислородной газификации температурой подогрева окислителя и составом дутья. [12]
Расчет равновесных составов растворов производится в той же последовательности, что и для газовых смесей. [13]
Расчет равновесного состава газа основан на следующих показателях: молекулярная формула углеводородов газифицируемого топлива, давление процесса газификации, температура процесса газификации, коэффициент избытка водяного пара, количество молей окиси углерода, прореагировавшей по реакции. [14]
Расчет равновесных составов конвертированного газа через систему полиномов с последующим получением их численных значений на ЭВМ применим такясе к случаю экзотермической конверсии с Выделением тепла реакция. [15]
Страницы: 1 2 3 4