Расчет - энергия - связь
Cтраница 3
Из сказанного ясно, что такие расчеты энергий связей в свободных радикалах в общем случае стали возможными только после вывода формулы для QCH в молекулах. До этого такие расчеты можно было провести в тех случаях, когда было известно ЛЯ образования радикала. [31]
Такой метод, оказавшийся исключительно удобным для расчета энергий связи комплексных ионов, должен быть достаточно надежным и при определении энергии перегруппировки растворителя. Для Fe3 равновесная величина равна 2 05 А и для расширения этого комплекса до г 2, 13 А также требуется 4 7 ккал. Очевидно, что конфигурация, при которой обе величины г равны 2 13 А, является наиболее благоприятной для электронного перехода. Однако требуемая для этого энергия несколько меньше 2 - 4 7 ккал, так как каждый исходный комплекс обладает некоторой нулевой энергией. [32]
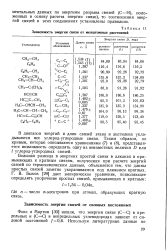 |
Зависимость энергии связи от межатомных расстояний. [33] |
С - Н), положенных в основу расчета энергии связи), то соотношения энергий связей в этих соединениях установлены правильно. [34]
Им соответствуют пять основных параметров, достаточных для расчета энергии связи любого алкана. [35]
Существует три основных модели, или подхода, к расчетам энергии связи электронов и объяснению химических сдвигов. Первый подход основывается на оценке эффективных зарядов атомов и сопоставлении их разности с химическими сдвигами для разных образцов. В самой грубой модели для оценки зарядов используется просто шкала электроотрицательностей. Например, заряд на атоме Ni ( II) в комплексах оценивают как разность электроотрицательностей атома и присоединенных к нему лигандов. Даже такая оценка удовлетворительно отражает разности зарядов и ход изменения химических сдвигов, а полуэмпирические методы квантовой химии ( ППДП, ЧПДП и др.) позволяют получить существенно лучшие результаты. [36]
Используя основные термодинамические соотношения, можно показать, что для расчета энергии связи влаги с материалом в качестве единственного критерия для классификации форм связи с материалом используют величину так называемой свободной энергии изотермического обезвоживания. Вследствие связывания воды с материалом понижается давление пара воды над его поверхностью, что приводит к уменьшению свободной энергии системы. [37]
Его сопоставление с вычисленным выше значением позволяет получить представление о степени точности расчетов энергий связей. К сожалению, в подобных расчетах приходится получать искомые величины как малые разности между двумя большими числами. [39]
Покажите, каким образом значение ДЯ в этой реакции можетбыть использовано для расчета энергии связи С-F, если известны все остальные энергии связей, требуемые для расчета. [40]
Преимущественное образование в рассматриваемом процессе дифенилалканов, а не алкилироваиных дифенилов подтверждается расчетом энергий связей в соответствующих соединениях. [41]
Хигучи, Ри и Эйринг [229] отчасти используют уравнение Полинга в своем расчете энергий связей атомов с поверхностью металлов. Названные авторы рассматривают долю ионной и ковалентной связи при хемосорбции; эти доли они находят из выражения для линейной комбинации волновых функций. Соответствующие интегралы авторы представляют для ковалентной связи при помощи уравнения Полинга ( без квадратичной поправки), а для ионной связи - через работу выхода, ионизационный потенциал, длину адсорбционной связи-и заряд электрона. В конечное уравнение входит также дипольный момент хемосорбционной связи. [42]
Покажите, каким образом значение АН в этой реакции может быть использовано для расчета энергии связи С - F, если известны все остальные энергии связей, требуемые для расчета. [43]
Покажите, каким образом значение ДЯ в этой реакции может быть использовано для расчета энергии связи С - F, если известны все остальные энергии связей, требуемые для расчета. [44]
В применении к пероксидам и спиртам данный подход использован в работе [129] для расчета энергий связей RO-H, RO-ОН, ROO - Н и RO-ОМе ряда соединений с кислородсодержащими функциональными заместителями. [45]
Страницы: 1 2 3 4
