Расчет - энергия - взаимодействие
Cтраница 2
Чтобы показать возможность проведения расчета энергии взаимодействия частиц по разным формулам, имеющимся в литературе, а также для сравнения полученных результатов, в таблицах приведены значения Um, полученные разными способами. [16]
Для окислов и интерметаллических соединений расчет энергии взаимодействия производился на основании теплот образования и энергии атомизации составляющих веществ. [17]
Однако в реальных молекулярных системах расчет энергии взаимодействия таким образом практически невозможен. Обычно в молекуле можно выделить почти обособленные области, несущие определенный заряд, причем эти области с достаточной степенью точности можно считать сферическими. [18]
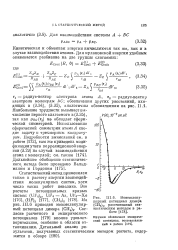 |
Межмолекулярный потепциал димера ( СН4 а, рассчитанный статистическим методом в работе. [19] |
Статистический метод применялся также к расчету энергии взаимодействия молекулярных систем, хотя число таких работ невелико. Согласие расчетного и эмпирического потенциалов [179] вполне удовлетворительное, особенно в области отталкивания. [20]
Для иллюстрации высказанного положения были проведены расчеты энергии взаимодействия радикала N02 с ( ЮО) - поверхностью модельного ГЦК-кристалла. На рис. 3 приведены рассчитанные модели адсорбции и полученные значения энергии. [21]
 |
Результаты квантовомеханического расчета молекулы водорода. [22] |
Гейтлером и Лондоном был также произведен квантовомеханичес-кий расчет энергии взаимодействия молекулы водорода с третьим атомом водорода. Так было дано теоретическое обоснование важнейшего свойства ковалентной связи - насыщаемости. [23]
 |
К расчету энергии взаимодействия. [24] |
Во-вторых, возможность свести задачу к расчету энергии взаимодействия между полубесконечной фазой и молекулой, удаленной на расстояние ft от нее, показывает, что AJ. I не зависит от взаимодействия ближайших соседей. Если бы нужно было проводить расчеты для ближайших соседей, то наличие дискретной структуры вещества потребовала бы прибегнуть к суммированию, которое затрудняет математические операции. [25]
Джонса; оно наиболее применимо при расчете энергии взаимодействия неполярных или малополярных молекул. [26]
Это выражение будет использовано нами при расчете энергий взаимодействия адсорбированных атомов или молекул с поверхностью при физической адсорбции последних на металлах и на угле, обусловленной неполярными силами Ван-дер - Ваальса. Как можно видеть, в этом выражении потенциальная энергия также обратно пропорциональна третьей степени расстояния. [27]
Для оценки достоверности полученного значения h0 проводят расчет энергии взаимодействия частиц золота на таком расстоянии между ними. Константу Гамакера, необходимую для такой оценки, находят по величине скр. [28]
Физические свойства легких газов, необходимые для расчета энергий взаимодействия, приведены в табл. 8.17. Специфичность цеолит-ных адсорбентов по отношению к молекулам данного адсорбата определяется величинами энергий взаимодействия разных типов. Отталкивание на малых расстояниях и дисперсионное притяжение осуществляются во всех случаях. [29]
Дебай в 1920 г. вывел выражение для расчета энергии взаимодействия полярной молекулы с неполярной. Под действием поля с напряженностью Е в нейтральной молекуле наводится диполь с моментом ( см. раздел 6.2.4) ц аЕ, а - поляризуемость нейтральной молекулы. [30]
Страницы: 1 2 3 4