Термодинамический расчет
Cтраница 2
Термодинамический расчет показывает, что эффективная удельная работа и эффективный КПД газотурбинного двигателя в разной степени зависят от соотношения давления воздуха в процессе сжатия в осевом компрессоре ( С) ГТУ. [16]
Термодинамические расчеты часто сравнивают с машиной, в которую загружают экспериментальные данные и получают требуемые результаты. Такое представление не следует принимать безоговорочно, так как разнообразие и исходных данных и задачах устанавливает определенные пределы для механизации термодинамического анализа. Но тем не менее это сравнение способствует более широкому взгляду на цель термодинамических расчетов. [17]
Термодинамические расчеты показывают, что удельная эффективная работа и эффективный КПД ГТД в разной степени зависят от С. При этом соответствующие значения С, по условию максимального значения КПД ГТД значительно выше. Так, если при возрастании наивысшей температуры цикла ГТУ от 750 до 950 С оптимальное значение С, при котором удельная работа двигателя максимальна, изменяется в узком диапазоне ( от 6 до 9), то диапазон изменения С при условии максимального КПД значительный-9... При наивысшей температуре цикла ГТУ более 900 - 950 С диапазон С значительно увеличивается. [18]
 |
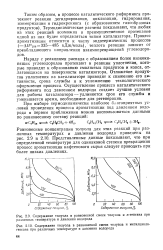
Равновесное содержание компонентов разложения [ % ( об. ] при различных температурах и содержании Нг SOt. [19] |
Термодинамические расчеты позволяют определить равновесный состав технологического газа, используемого для дальнейшей переработки в серную кислоту. [20]
Термодинамические расчеты замечательны тем, что одно и то же значение термодинамической характеристики может быть получено несколькими независимыми способами. [21]
Термодинамические расчеты свидетельствуют о высокой термодинамической вероятности растворения золота в гидросульфидных растворах. При гидрометаллургической обработке руд, где присутствие кислорода неизбежно, более вероятно взаимодействие золота с гидросульфидом и кислородом. Реакция в данном случае аналогична основной реакции процесса цианирования, описываемой уравнением Эльснера, и близка к ней по энергетическому эффекту. При характеристике механизма этого процесса необходимо учитывать, что кислород может выступать или как приемник электронов, отнимаемых у золота, или, взаимодействуя с сульфидными и гидросульфидными ионами, превращать их в соответствующие полисульфидные соединения, обладающие окислительными свойствами и способные взаимодействовать с золотом даже в отсутствие кислорода. [22]
Термодинамические расчеты показывают, что любая из этих реакций возможна и преимущественное протекание одной из них будет определяться типом катализатора. Процесс ароматизации относится к числу эндотермических процессов ( - АЯ 298 335 - 485 кДж / моль), теплота реакции зависит от преобладающего направления взаимопревращений углеводородов. [24]
Термодинамические расчеты для идеального газа с ky 1 могут выполняться и с помощью газодинамических функций. [25]
Термодинамический расчет позволяет заранее определить принципиальную невозможность протекания того или иного процесса и тем самым избежать постановки опытов, которые будут обречены на неудачу. Однако термодинамический анализ, определяя движущую силу процесса, позволяет указать только направление последнего. Для нахождения же скорости его протекания надо знать также величину сопротивления, что связано с рассмотрением механизма процессов и поэтому термодинамикой не изучается. [26]
Термодинамические расчеты показали, что при наличии восстановительной среды ( углерода) основная масса РЗЭ в газовой фазе находится в виде одноатомных молекул металла. [27]
Термодинамические расчеты показывают, что образование гидразина возможно лишь при определенных значениях энергии связи азота в комплексе и определенной структуре комплекса и значениях потенциалов восстановителя. [28]
Термодинамические расчеты показывают, что уже при 25 С равновесие реакции сдвигается вправо. При 250 С конверсия метанола должна проходить почти до конца. В области температур 25 - 300 С наряду с основной реакцией возможны другие процессы, приводящие к образованию побочных продуктов в газовой смеси: окиси углерода, формальдегида и пр. Основной опасной примесью будет окись углерода, содержание которой растет с увеличением температуры и уменьшением парциального давления водяного пара. [29]
Термодинамические расчеты показывают, что для достижения достаточно высокой степени гидрирования ароматических углеводородов и снижения содержания их в моторных топливах, можно идти не по пути повышения общего давления в реакционной системе, а по пути подбора высокоактивных катализаторов, повышающих скорость достижения равновесных составов, определяемых термодинамическими условиями. [30]
Страницы: 1 2 3 4