Термодинамический расчет
Cтраница 3
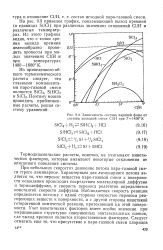 |
Зависимость состава паровой фазы от состава исходной смеси С1 / Н при Г1450 К. [31] |
Термодинамические расчеты, конечно, не учитывают кинетических факторов, которые вызывают некоторые отклонения от описанного поведения системы. [32]
 |
Схема тигля для получения кристаллов a - SiC полупроводникового качества по методу Лели. / - графитовый тигель. 2 - исходная масса SiC. 3 - перекристаллизованный SiC. [33] |
Термодинамический расчет этой реакции показывает, что получение карбида кремния может иметь место только при температурах, превышающих 700 С. Однако образование SiC при температуре 1000 С столь незначительно, что процесс проводится при 1600 - 1700 С. Процесс осуществляют в герметичном кварцевом реакторе, внутри которого располагается графитовая пластинка, нагреваемая током до нужной температуры. В реактор подаются пары CH3SiCl3, используя в качестве газа-носителя чистый водород; молекулы CH3SiCl3 диссоциируют на нагретой поверхности, которая покрывается слоем мелких кристаллов B-SiC. Цвет полученных кристаллов изменяется в зависимости от температуры подложки, так как при этом изменяется соотношение компонентов, выделяющихся на подложке. [34]
Термодинамический расчет [79] процесса при температурах, применяемых в промышленности ( 400 - 500 С), показывает его практическую необратимость. [35]
Термодинамические расчеты этой системы были проведены для интервала температур 1000 - 1700 К, коэффициента избытка сероводорода 1 5 - 0 5 и давлений 0 01 - 1 0 МПа. [37]
Термодинамические расчеты показали принципиальную возможность хлорирования безуглеродистого феррохрома по уравнениям ( I-XIII) - изобарный потенциал всех указанных реакций имеет большое отрицательное значение. [38]
Термодинамические расчеты свидетельствуют также о возможности реакций титана с CaFa и особенно с NaF. Однако по экспериментальным данным количество кальция и натрия, переходящих в металл шва, весьма незначительно. Содержание кальция в шве возрастает на тысячные доли процента по сравнению с его концентрацией в основном металле, в котором кальций присутствует в виде примеси. Химический анализ не улавливает перехода натрия в наплавленный металл. Однако наблюдается измельчение структуры металла шва при сварке под флюсами, содержащими фторид натрия. [39]
Термодинамические расчеты показывают, что для достижения подобным путем достаточно высокой степени превращения метана и получения водорода достаточной чистоты необходимы очень высокие температуры ( порядка 1500) и весьма значительный расход тепла. С понижением температуры степень разложения метана прогрессивно снижается и водород обогащается непрореагировавшим метаном. [40]
Термодинамические расчеты и опыт показывают, что особенности поведения вещества в критической точке проявляются в значительном интервале составов по обе стороны от критическою состава, а также в значительном интервале температур при удалении от критической температуры в гомогенную область. [41]
 |
Константы равновесия реакций ( VI-10 - ( VI-13 поглощения сероорганических соединений окисью цинка. [42] |
Термодинамические расчеты показывают, что реакции поглощения сероорганических соединений окисью цинка при 400 - 450 С практически необратимы, следовательно, возможна полная очистка газа от этих соединений. Как окись цинка, так и продукт реакции - сульфид цинка, в восстановительной атмосфере очищаемого газа при температуре до 400 - 500 С вполне стабильны. [43]
Термодинамический расчет показывает возможность протекания отдельных стадий процесса и его глубину. [44]
Термодинамический расчет указывает на невозможность образования свободной перекиси натрия по реакции ( 42) и не может объяснить наблюдаемое присутствие Na2O2 в прокаленной массе, полученной из хромитовых шихт. Очевидно в печах Na2O2 образуется другим путем и находится не в свободном, а в растворенном состоянии. [45]
Страницы: 1 2 3 4