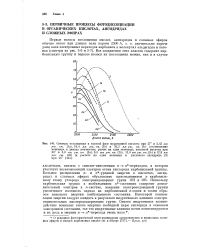
Большее расщепление
Cтраница 1
Большее расщепление п - и я - уровней энергии в кислотах, ангидридах и сложных эфирах обусловлено присоединением к карбонильному атому углерода электронодонорных групп ОН и OR. Поскольку карбонильная группа в возбужденном я - состоянии содержит дополнительный электрон в я-системе, введение электронодонорной группы увеличивает плотность заряда на карбонильной я-связи и таким образом повышает энергию возбужденного состояния. Некоторой компенсации энергии следует ожидать в результате индуктивного влияния электроотрицательных кислородсодержащих групп. [2]
 |
Сректры поли ( винилметилового эфира. [3] |
Таллий вызывает очень большие расщепления в спектре этиль-ных групп, и полная развязка метильных и метиленовых протонов уже невозможна. [4]
Предположим, что большее расщепление обусловлено азотом. [5]
Для ионов с большим расщеплением в нулевом поле наблюдаются только некоторые из разрешенных переходов. [6]
Почему группа CN вызывает большее расщепление молекулярных орбиталей, чем F. Как уже указывалось в предыдущем разделе, равное обобществление электронов между центральным атомом и ли-гандом ( соответствующее в этой картине значениям а b с / 1 / 2) приводит к слишком большой концентрации отрицательного заряда на атоме железа. При этом разрыхляющие состояния ф и ф приближаются к атомным состояниям и ыхз - У2 и оказываются ближе по энергии к 3dxv, tysdyz и Однако, как упоминалось в предыдущем разделе, в случае цианидных комплексов заряд может смещаться от железа к лиганду благодаря образованию дативных я-связей. Вследствие такого смещения заряда становятся возможными несколько большие значения а, b и с, в результате чего происходит большее расщепление молекулярных орбиталей различных типов. Однако введение дативных связей усложняет всю картину, так как при этом несвязывающие орбитали вовлекаются в образование молекулярных орбиталей. Орбитали 3dx, tysdyz и tysd комбинируются с орбиталями лигандов так же, как это было описано при рассмотрении в методе валентных связей, с образованием вместо исходных несвязывающих орбиталей трех новых связывающих и трех разрыхляющих орбиталей. [7]
Иначе получается в случае больших расщеплений. Когда количество электронов превышает число орбиталей нижнего подуровня, например для октаэдрического поля лигандов станет больше трех, следующие электроны занимают оставшиеся места на орбиталях нижнего подуровня, преодолевая энергию оттал - кивания с уже имеющимися там электронами. Спины каждой пары электронов одной орбитали антипараллельны. Суммарный спин системы понижается. Величина спина характеризует магнитные свойства. Состояние с высоким спином соответствует парамагнитным, а с низким спином - диамагнитным комплексам. [8]
Иначе получается в случае больших расщеплений. Когда количество электронов превышает число орбиталей нижнего подуровня, например для октаэдрического поля лигандов станет больше трех, следующие электроны занимают оставшиеся места на орбиталях нижнего подуровня, преодолевая энергию отталкивания с уже имеющимися там электронами. Спины каждой пары электронов одной орбитали антипараллельны. Суммарный спин системы понижается. Величина спина характеризует магнитные свойства. Состояние с высоким спином соответствует парамагнитным, а с низким спином - диамагнитным комплексам. [9]
 |
Спектр радикала NH2. [10] |
Предположив, что водород обусловливает большее расщепление, постройте диаграмму, аналогичную изображенной на рис. 10 - 7, для объяснения этого спектра. [11]
Никакого объяснения механизма, вызывающего большие расщепления полос и изменения интенсивностей в спектре бензола, предложено не было. Дипольное взаимодействие не может являться основной причиной, так как запрещенные в газовой фазе основные полосы чрезвычайно низкой интенсивности и, следовательно, соответствующие низкому дипольному моменту перехода расщепляются примерно так же, как и разрешенные полосы основных колебаний довольно высокой интенсивности. Изобилие детальной информации, надежно установленная структура кристалла, отсутствие собственного дипольного момента молекулы и наличие нескольких основных полос, индуцированных полем кристалла, делают спектр бензола заманчивым объектом для интерпретации. [12]
Лиганды, являющиеся тг-акцепторами, вызывают большее расщепление rf - уровня; лиганды, являющиеся т-донорами, наоборот, вызывают малое расщепление rf - уровня. [13]
Рассмотренные расщепления второго порядка наблюдаются только при сравнительно больших расщеплениях. И они указаны здесь, чтобы предупредить читателя о такой возможности. Однако расщепление второго порядка не дает какой-либо информации, которую нельзя было бы получить из спектров первого порядка. [14]
Парамагнитные ионы со спином 5 V2 обычно имеют большие расщепления в нулевом поле, что приводит к сильному уширению спектров. [15]
Страницы: 1 2 3 4