Спин-орбитальное расщепление
Cтраница 3
В оболочке 1 / г, как и в lg, спин-орбитальное расщепление настолько велико, что состояния l / iu / 2 и 1 / гв / 2 принадлежат разным оболочкам. В атоме они относятся к третьей оболочке, а в ядре за счет короткодействия ядерных сил - к пятой. При заполнении пятой оболочки в ядре оказывается 82 нуклона соответствующего сорта. [31]
 |
Переход от рассел-саундерсовой связи к. - / - связи. [32] |
Для оболочек, заполненных наполовину, в первом порядке теории возмущений спин-орбитального расщепления термов вообще не получается; экспериментально наблюдается очень слабое расщепление, обусловленное эффектами второго порядка. [33]
Если можно пренебречь изменениями знаменателей Ей - Е л за счет возможного спин-орбитального расщепления состояний а /), то ясно, что значения матричных элементов ( г j (: s) [ см. ( 43) ] не изменяются при преобразовании состояний а /), диагонализирующем гамильтониан спин-орбитального взаимодействия. [34]
В принципе возможно оценить степень ионной связи в соединениях III-V по величине спин-орбитального расщепления валентной зоны этих кристаллов ( см. гл. Поскольку спин-орбитальное взаимодействие осуществляется в глубоких оболочках атома, образование кристалла не может на нем существенно сказаться. Например, величина спин-орбитального расщепления валентной зоны в кристалле германия в 1 45 раза превышает величину расщепления р-функций атома германия. [35]
У - L, I - S и Г - J совпадает с формулой (19.4) для спин-орбитального расщепления терма. [36]
Наличие структуры в первой полосе собственного поглощения бромистых и йодистых соединений щелочных металлов Гильш и Поль [1] приписывали спин-орбитальному расщеплению основного состояния атомов брома и иода и полагали, что только малая разность энергии между компонентами дублета 2Р и 2Р в случае хлористых соединений не позволяет обнаруживать также и у них дублетной структуры. Однако спин-орбитальной связью в атомах галоида может быть обусловлено не более двух максимумов, тогда как первая полоса поглощения, по-видимому, состоит из большего числа компонент. [37]
Спин-орбитальное расщепление зон энергии, образованных из р-уровней, может быть только дублетным, чистые s - зоны не имеют спин-орбитального расщепления. В полупроводниках IV группы и в соединениях элементов типа A1HBV и AUBVI спин-орбитальное расщепление наблюдается для валентной зоны. При фиксированном элементе В величина расщепления остается практически постоянной. Это находится в хорошем соответствии со сказанным в § 26 о характере образования зон энергии соединений А У. [38]
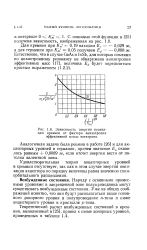 |
Зависимость энергии ионизации примеси от фактора анизотропии эффективной массы электрона. [39] |
Удовлетворительная теория акцепторных уровней в кремнии отсутствует, так как в этом случае энергия ионизации акцептора по порядку величины равна значению спин-орбитального расщепления. [40]
Хщ) - доли времени, которые валентный электрон находится возле Ill-атома и V-атома соответственно; Дщ и Ду - величины спин-орбитального расщепления в этих атомах, а Дш у-величина расщепления в кристалле. В табл. 4 приведены значения величины спин-орбитального расщепления для атомов некоторых из элементов III и V групп. [41]
В комплексах ионов переходных металлов член S-D-S используют для описания любого эффекта, который снимает спиновое вырождение, включая дипольные взаимодействия и спин-орбитальное расщепление. Низкосимметричное кристаллическое поле часто приводит к большим эффектам нулевого поля. [42]
R, при которой совершается переход, аппроксимируется зависимостью A CR -, п 1, и в области перехода значительно превышает спин-орбитальное расщепление атомного уровня. Вычислить сечение рассматриваемого перехода, усредненное по направлениям столкновения. [43]
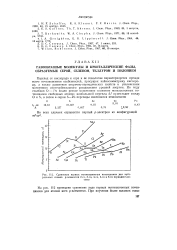 |
Сравнение первых ионизационных потенциалов для нейтральных атомов р-элементов 2-го, 3-го, 4-го, 5-го и 6-го периодов Системы. [44] |
Переход от кислорода к сере и ее гомологам характеризуется прежде всего исчезновением особенностей, присущих кайносимметрику кислороду, а также развитием вторично-периодических свойств и увеличением магнитного спин-орбитального расщепления уровней энергии. [45]
Страницы: 1 2 3 4