Рауля
Cтраница 1
Рауля), во всем интервале концентраций остаются не только один и тот же порядок изменения состава, но и постоянное численное значение температурного коэффициента. [1]
Рауля и Бабо), неизменным остается во всех концентрациях раствора не только порядок изменения состава, но и численное значение температурного коэффициента. [2]
Рауля ( ид СаоСао) так как повышение температуры увеличивает тепловой беспорядок молекул и приближает систему к идеальному состоянию. [3]
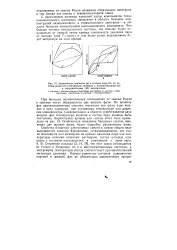 |
Зависимость давления ( а и состава пара ( б от состава жидкости в бинарных системах с положительным ( т и отрицательным ( М азеотропами. [4] |
Рауля возможно образование азеотропа и тем ближе его состав к эквимолекулярной смеси. [5]
 |
Изотермические диаграммы давления пара двойных Ж. с.. а - дли идеальной системы. б - без гшстремумов. в - с максимумом. г - с минимумом. [6] |
Рауля, согласно к-рому при постоянной темп-ре давление пара любого компонента пропорционально выраженной в мольных долях его концентрации в жидкости, причем коэфф. [7]
Рауля с введением поправки на образование твердых растворов никак не связан с законом граничного хода равновесного коэффициента распределения. [8]
 |
Определение осмотического давления. [9] |
Рауля никогда не выполняется. [10]
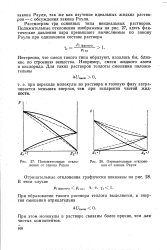 |
Положительные отклот нения от закона Рауля.| Отрицательные отклонения от закона Рауля. [11] |
Рауля, так же как изучение идеальных жидких растворов - с обсуждения закона Рауля. [12]
Рауля не вполне справедлив в реальных условиях опыта. Для того чтобы внести поправки в вычисления, вызванные как этими, так и другими возможными ошибками, необходимо поступать следующим способом: в случае каждого образца повышение температуры кипения определяют для нескольких концентраций растворенного вещества. На практике такие определения проводят, сравнивая температуру кипения чистого растворителя в одном эбуллиометре с температурами кипения, определяемыми в другом эбуллиометре, ряда растворов, полученных добавлением к растворителю последовательных порций исследуемого образца. Первый эбуллиометр служит, так сказать, в качестве точного барометра. Пересечение этой прямой с осью молекулярного веса дает молекулярный вес образца. [13]
Рауля), или требует снижения давления кипения, если необходимо сохранить температуру кипения. Во-вторых, увеличение концентрации масла в растворе увеличивает вязкость раствора по сравнению с вязкостью рабочего тела, что ухудшает коэффициент теплоотдачи со стороны рабочего тела. [14]
Рауля, пропорциональное количеству растворенного вещества. Этой точке, Как видно из рисунка, соответствует более низкая температура плавления, чем для чистого вещества. [15]
Страницы: 1 2 3 4 5