Рауля
Cтраница 2
Рауля соответствуют положительные, а положительным отклонениям от закона Рауля - отрицательные отклонения поверхностного натяжения от идеальности. [16]
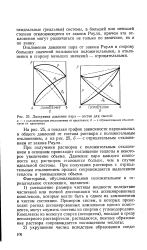 |
Диаграмма давление пара - состав для смесей. а - с положительным отклонением от идеальных. б - с отрицательным отклонением от идеальных. [17] |
Рауля, причем эти отклонения могут различаться не только по величине, но и по знаку. [18]
Рауля, N н о н оК Поскольку Яд в - РН необходимые для образования гидратов критические значения У. [19]
Рауля вызывают появление экстремума на кривой общего давления. [20]
 |
Зависимость давления ( а и состава пара ( б от состава жидкости в бинарных системах с положительным ( т и отрицательным ( М азеотропами. [21] |
Рауля возможно образование азеотропа и тем ближе его состав к эквимолекулярной смеси. [22]
Рауля, Авторы объясняют это образованием химических соединений между теллуром и селеном в жидкой фазе и паре. [23]
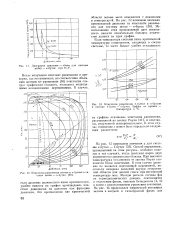 |
Константы равновесия метана и и-бутана в системе метан - н-бутан.| Константы равновесия 1-бутеиа и н-бутана в системе 1-бутен - н-бутан. Цифры па кривых - температура в С. [24] |
Рауля [31], и константы, полученной экспериментально. [25]
Рауля и вычисляемая из ( 24) по известному значению у, для одной из примесей. При выводе ( 24) было принято, что взаимодействие в конденсированной фазе описывается теми же выражениями, что и в газе. При этом предполагалось, что ориентацион-ное взаимодействие аддитивно. Это, как уже было отмечено, не строго. [26]
Рауля для растворенного вещества не соблюдается. [27]
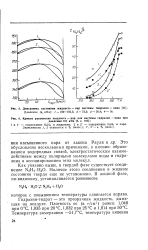 |
Диаграмма состояния жидкость - пар системы гидразин - вода. Давление ( в, кПа. / - 100 - 102 5. 2 - 72 2. 3 - 36 4. 4 - 16.| Кривые равновесия жидкость - пар для системы гидразин - вода при. [28] |
Рауля и др. Это обусловлено несколькими причинами, а именно: образованием водородных связей, электростатическим взаимодействием между полярными молекулами воды и гидразина и ассоциированием этих молекул. [29]
Рауля, а еще лучше вычислить по уравнению ( 1.165 а), если известны значения А; увеличение же летучести вещества вследствие наложения на него давления можно вычислить по уравнению (1.157) с применением мольного объема вещества вместо его парциального мольного объема. [30]
Страницы: 1 2 3 4 5